
����Ŀ�����ĺϳ���Ŀǰ�ձ�ʹ�õ��˹��̵�������
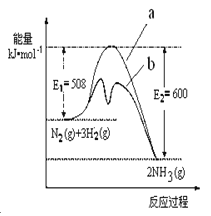
(1) ����ͼ�ṩ����Ϣ��д���÷�Ӧ���Ȼ�ѧ���� ����ͼ�������� ������a�� ����b������ʾ��������ý�������仯���ߡ�
(2) �ں�����������������������˵��������Ӧ�Ѵ�ƽ�����
A��3v(H2)��=2v(NH3)��
B����λʱ��������n mol N2��ͬʱ����2n molNH3
C��������������ܶȲ���ʱ��ı仯���仯
D��������ѹǿ����ʱ��ı仯���仯
���𰸡�(1)N2(g)+3H2(g)![]() 2NH3(g)��H=-92kJ/mol��b(2)BD
2NH3(g)��H=-92kJ/mol��b(2)BD
��������
�������������ͼ���������Ӧ����H=508-600=-92KJ/mol�� (1) N2(g)+3H2(g) ![]() 2NH3(g) ��H=-92kJ/mol��(2) A��3v(H2)��=2v(NH3)�� ����֮�ȵ���ϵ������������B����λʱ��������n mol N2��ͬʱ����2n molNH3 ��B��ȷ��C����Ӧǰ����������������䣬������������䣬�ܶ��κ�ʱ��������������ܶȲ���ʱ��ı仯���仯�����ж��Ƿ�ƽ����D����Ӧǰ���������������ȣ�������ѹǿ����ʱ��ı仯���仯��D��ȷ��
2NH3(g) ��H=-92kJ/mol��(2) A��3v(H2)��=2v(NH3)�� ����֮�ȵ���ϵ������������B����λʱ��������n mol N2��ͬʱ����2n molNH3 ��B��ȷ��C����Ӧǰ����������������䣬������������䣬�ܶ��κ�ʱ��������������ܶȲ���ʱ��ı仯���仯�����ж��Ƿ�ƽ����D����Ӧǰ���������������ȣ�������ѹǿ����ʱ��ı仯���仯��D��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�������һ��ʵ����̽��Ԫ�������ɡ���ͬѧ����Ԫ�طǽ��������Ӧ��ۺ�����֮��Ĺ�ϵ���������ͼװ����һ�������̼��Ԫ����C��Si�ķǽ�����ǿ���Ƚϵ�ʵ���о�����ͬѧ�������ͼװ������֤±��Ԫ�����ʵĵݱ���ɡ�

����ͼ�ش�
(1)��ͬѧ���ʵ���������____________________________________��
(2)д��ѡ�õĻ�ѧ�Լ���B____________��������Ϊ___________��
(3)C�з�Ӧ�����ӷ���ʽΪ____________________________________________��
����ͼ�ش�
��ͬѧ��ʵ����̣�
��.���ɼУ�����a���μ�Ũ���ᡣ
��.��B��C�е���Һ����Ϊ��ɫʱ���н����ɼС�
��.��B����Һ�ɻ�ɫ��Ϊ�غ�ɫʱ���رջ���a��
��.����b��������C����Һ����D�У��رջ���b��ȡ��D�����ú�CCl4����Һ��Ϊ�Ϻ�ɫ��
(4)д��B����Ӧ�����ӷ���ʽ ___________________________________________��
(5)A����֤������������ǿ�ڵ��ʵ��������_____________________��
(6)���̢�ʵ���Ŀ����_________________________��
(7)�ۺϼס�����ͬѧ��ʵ��ó��Ľ����ǣ�ͬ����Ԫ�ش��ϵ���Ԫ�صķǽ�����������ԭ����___________________________________________���Դ�ԭ�ӽṹ�ǶȽ��ͣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ��ԭ���ԭ�������˶��ֵ�أ������㲻ͬ����Ҫ������ÿС���еĵ�ع㷺ʹ�����ճ���������Ϳ�ѧ�����ȷ��棬����������ṩ����Ϣ��ա�
��1�������ڷŵ�ʱ��ԭ������ã��ڳ��ʱ����ص����á�Ǧ�����ڷŵ�ʱ�����ĵ�ط�ӦʽΪ��Pb+PbO2+2H2SO4��2PbSO4+2H2O��������ӦʽΪ________________________________����Ӧһ��ʱ���������_________������ء����١����䡱��
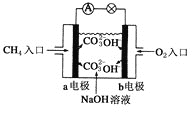
��2��ȼ�ϵ����һ�ָ�Ч�������ѺõĹ���װ�ã���ͼ�Ǽ���ȼ�ϵ��ԭ��ʾ��ͼ���õ�ؼ��ĸ��缫��Ӧʽ�ǣ�________________________����״���£�2.24L�ļ���ȫ����Ӧ����ת��________ mol��
��3������Ƭ��ͭƬ�õ����������ֱ����Ũ�����У�a�飩�Ͳ����ռ���Һ�У�b�飩�����γ���ԭ��أ���a��ԭ����У���������Ϊ______��д��b������ռ���Һ���γ�ԭ��صĸ�����Ӧʽ��_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ؿ�����������һ����ľ�����ij�������( )
A. ���ٸ��˾���֧�� B. ��Լľ�ģ�����ɭ��
C. ���ٹ������� D. �Ʒ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʱ��0.1mol/L��һԪ��HA��ˮ����0.1%�������룬���������������
A����Һ��PH��4
B�������¶ȣ���ҺPH����
C������ĵ���ƽ�ⳣ��Ϊ1��10��7
D����HA�����c(H+)ԼΪˮ���������c(H+)��106��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2 molA��2 molB�����2 L���ܱ������У�������Ӧ��2A(g)��3B(g)![]() 2C(g)��zD(g)��
2C(g)��zD(g)��
��2 s��Ӧ�ﵽƽ�⣬A��ת����Ϊ50%�����v(D)��0.25 mol��L��1��s��1�����㣺
��1����C��ʾ�ķ�Ӧ����v(C)�� mol��L��1��s��1
��2��z��
��3��B��ת����Ϊ
��4��Cƽ��ʱ�����ʵ���Ϊ mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ԭ���ڹ�ҵ���й㷺Ӧ�á���ͼ��һ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ������
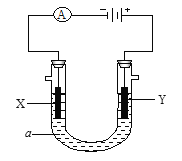
��ش��������⣺
(1) ��X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
��������X���ϵĵ缫��Ӧʽ�ǣ� ��
��X�������۲쵽�������ǣ� ��
��Y�缫�ϵĵ缫��Ӧʽ�ǣ� ��
����õ缫��Ӧ����ķ����ǣ� ��
(2) ��Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ����ǣ� ���缫��Ӧʽ�ǣ� ��
��Y�缫�IJ����ǣ� ���缫��Ӧʽ�ǣ� ��
��˵�������ʷ����ĵ缫��Ӧ����д����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ǧ(PbSO4)�㷺Ӧ��������Ǧ���ء���ɫ���ϵȡ����÷�Ǧ��( PbS)ֱ���Ʊ�����Ǧ��ĩ���������£�
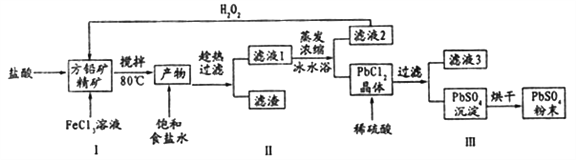
��֪��(i) PbCl2 (s)+2C1-(aq)=PbCl42-(aq) ��H>0
(ii)�й����ʵ�Ksp�ͳ���ʱ��pH���£�
���� | Ksp | ���� | ��ʼ����ʱpH | ��ȫ����ʱpH |
PbSO4 | 1.0��10-8 | Fe(OH)3 | 2.7 | 3.7 |
PbCl2 | 1.6��10-5 | Pb(OH)2 | 6 | 7.04 |
��1������I��Ӧ�����������Թ۲쵽����ɫ�������ɣ���д�������ӷ���ʽ___________��
��2���û�ѧƽ���ƶ���ԭ�����Ͳ������ʹ�ñ�ˮԡ��ԭ��____________��
��3�����������������п���ѭ�����õ�������______________��
��4��д���������PbCl2����ת��ΪPbSO4���������ӷ���ʽ________________��
��5��Ǧ��ұ�����ӹ���ʹˮ�����ؽ���Ǧ�ĺ����������������Ⱦ��ij�������Ʊ���һ��������Ǧ������EH��ʾ��������Чȥ��ˮ�еĺ���Ǧ����Ǧ��������Ҫ�����ķ�ӦΪ��2EH(s)+Pb2+![]() E2Pb(s)+2H+������Ǧ������ʵ�pH��ΧΪ____�����ţ�
E2Pb(s)+2H+������Ǧ������ʵ�pH��ΧΪ____�����ţ�
A.4��5 B.6��7 C.9��10 D.11��12
��6��PbSO4�ȼ����ؿ���������������Ĺ�����Դ�������ṹ��ͼ��ʾ��������Ϊ����ʵ���ˮLiCl-KC1������������ں�ؼ���˲��������ܡ��õ���ܷ�ӦΪPbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb��

�ٷŵ�����У�Li+��_______�ƶ����������������������
�ڸ�����ӦʽΪ_____________��
�۵�·��ÿת��0.2mol���ӣ�����������_________g Pb��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ�ã�ͨ�����Cu��������Һ��ɫ�������˵����ȷ����
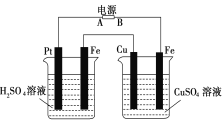
A��A��������Cu����
B�����ձ���Һ�����ձ���Һ��pH����С
C�����ձ�Pt�������ձ�Fe���ĵ��������ʵ���֮��Ϊ1:1
D�����ձ���ҺŨ�ȱ�����ձ���ҺŨ�Ȳ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com