
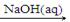 NaAlO2(aq)
NaAlO2(aq) 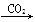 Al(OH)3
Al(OH)3 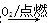 SO3
SO3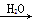 H2SO4
H2SO4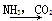 NaHCO3
NaHCO3 Na2CO3
Na2CO3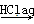 FeCl3(aq)
FeCl3(aq)  无水FeCl3
无水FeCl3 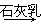 Mg(OH)2
Mg(OH)2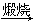 MgO
MgO| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
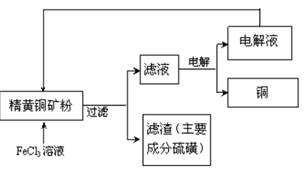
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝热反应是炼铁最常用的方法 |
| B.高纯度的硅单质用于制作光导纤维 |
| C.二氧化氯具有强化性,可用于自来水的杀菌消毒 |
| D.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
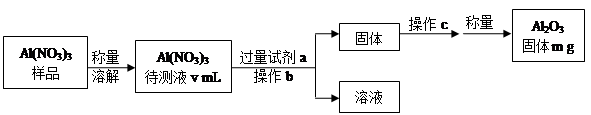

| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
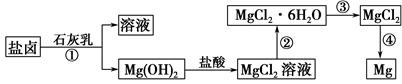
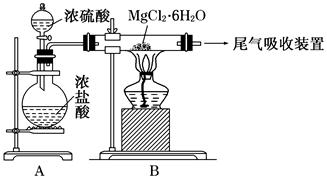
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
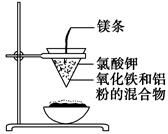
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.Ca(ClO)2(aq)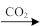 HClO(aq) HClO(aq) HCl(aq) HCl(aq) |
B.H2SiO3 SiO2 SiO2 SiCl4 SiCl4 |
C.Al2O3 NaAlO2(aq) NaAlO2(aq)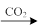 Al(OH)3 Al(OH)3 |
D.Fe2O3 Fe2(SO4)3(aq) Fe2(SO4)3(aq) 无水Fe2(SO4)3 无水Fe2(SO4)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com