
下列说法正确的是
A.100°C时,某溶液pH=6,则该溶液一定显酸性
B.25℃时,0.lmol/L 的 NaHSO3溶液 pH=4,溶液中 c(SO32-)<c(H2SO3)
C.25℃时,pH=3的硫酸溶液与pH=11的氨水等体积混合,所得溶液呈酸性
D.室温下,10mL0.1moI/LCH3COOH溶液与5mL0.1mol/LNaOH溶液混合,所得溶液中有:
2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-)
科目:高中化学 来源:2017届湖南省长沙市高三上月考四化学卷(解析版) 题型:选择题
下列实验能达到预期目的的是
编号 | 实验内容 | 实验目的 |
A | 取两只试管,分别加人4 mL 0.01 mol/L KMnO4酸性溶液,然后向一只试管中加入 0.1 mol/L H2C2O4溶液2 mL,向另一只试管中加入0.1 mol/L H2C2O4溶液 4 mL,记录褪色时间 | 证明草酸浓度越大,反应速率越快 |
B | 向含有酚酞的Na2CO3溶液中加入少量 Ba(OH)2固体,观察溶液颜色变化 | 证明Na2CO3溶液中存在水解平衡 |
C | 向10 mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol/L FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的 Ksp:Mg(OH)2> Fe(OH)3 |
D | 测定相同条件等物质的量浓度的 Na2SO4溶液与Na2CO3溶液的pH,后者较大 | 证明非金属性S>C |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:推断题
有机物A~F有如下转化关系:
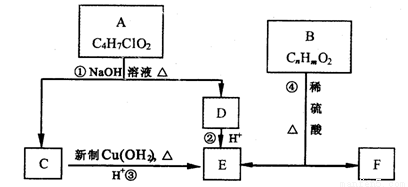
已知一个碳原子上连有两个羟基时不稳定,转化如下:
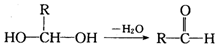
请回答:
(1)A的结构简式为: ;④的反应类型 ;
(2)C与新制Cu(OH)2的化学方程式为 ;
(3)已知B的摩尔质量为162g/mol,完全燃烧的产物中n(CO2):n(H2O)=2:1,B的分子式为 。
(4)F是生产高分子光阻剂的主要原料,特点如下:
①能发生加聚反应;②含有苯环且苯环上一氯取代物只有两种;③遇FeCl3显紫色
F与浓溴水反应的化学方程式 ;
B与NaOH反应的化学方程式 ;
(5)F的一种同分异构体G含苯环且能发生银镜反应。写出一种满足条件的G的结构简式 ;
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:选择题
盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是 ( )
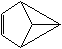
A.盆烯是苯的一种同分异构体
B.盆烯分子中所有的碳原子不可能在同一平面上
C.盆烯是乙烯的一种同系物
D.盆烯在一定条件下可以发生加成反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上阶段测二化学卷(解析版) 题型:选择题
室温下,用0.100mol﹒L-1NaOH溶液分别滴定20.00ml0.100mol﹒L-1的盐酸和醋酸,

A.Ⅰ表示的是滴定盐酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C.V(NaOH)=20mL时,两份溶液中c(Cl-)=c(CH3COO-)
D.V(NaOH)=10mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上阶段测二化学卷(解析版) 题型:选择题
下列关于电解质溶液的正确判断的是
A.在pH=12的溶液中,Al3+、Cl-、HCO3-、Na+可以大量共存
B.在pH=0的溶液中,Na+、NO3-、SO32-、K+可以大量共存
C.由0.1 mol/L —元碱BOH溶液的pH=10,可推知BOH溶液存在BOH B++OH-
B++OH-
D.pH =2的一元酸和pH =12的一元强碱等体积混后溶液一定存在:c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考二化学试卷(解析版) 题型:填空题
将等物质的量的A、B混合于2  L的密闭容器中,发生如下反应:3A(g) + B(g)
L的密闭容器中,发生如下反应:3A(g) + B(g)  xC(g) + 2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g) + 2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=________mol;
(2)B的平均反应速率v(B)=________mol/(L·min);
(3)x的值为________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:实验题
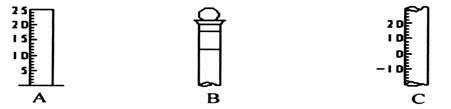
(1)请写出下列仪器的名称:A ,B ,C 。
(2)仪器B上标记有 (填序号)。
①质量 ②温度 ③刻度线 ④浓度 ⑤容积
Ⅱ.现用98%的浓H2SO4(密度为1.84g/cm3)来配制480mL0.2mol/L的稀H2SO4。
有关操作为:①计算所需浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释、冷却 ④转移、洗涤 ⑤定容 ⑥摇匀。回答下列问题
(3)应用量筒量取的浓硫酸体积是 mL,实验中所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还有 。
(4)第③步中稀释浓硫酸的操作是 。
(5)将所配制的稀H2SO4进行测定,发现实际浓度大于0.2mol/L。请你分析下列哪些操作会引起所配浓度偏大(填写字母) 。
A.用量筒量取浓硫酸时,仰视量筒的刻度 |
B.容量瓶未干燥即用来配制溶液 |
C.浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容 |
D.往容量瓶转移时,有少量液体溅出 |
E.烧杯未进行洗涤
F.在容量瓶中定容时俯视容量瓶刻度线
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上12月考前测试化学卷(解析版) 题型:实验题
测血钙的含量时,可将2.0 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4
 沉淀。将沉淀用稀硫酸处理得H2C
沉淀。将沉淀用稀硫酸处理得H2C 2O4后,再用酸性KMnO4溶液滴定,
2O4后,再用酸性KMnO4溶液滴定, 氧化产物为CO2,还原产物为Mn2+,若终点时用去20.
氧化产物为CO2,还原产物为Mn2+,若终点时用去20. 0 mL 1
0 mL 1 .0×10-4 mol·L-1的KMnO4溶液。
.0×10-4 mol·L-1的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式 。
(2)判断滴定终点的方法是 __________________ 。
(3)计算:血液中含钙离 子的浓度为 __________ g·mL-1。
子的浓度为 __________ g·mL-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com