
【题目】始祖鸟烯形状宛如一只展翅飞翔的鸟,其键线式结构表示如下,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是( )
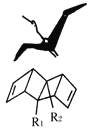
A.始祖鸟烯与乙烯互为同系物
B.若R1=R2=甲基,则其化学式为C12H14
C.若R1=R2=甲基,一定条件下烯烃双键碳原子上的氢也能被取代,则始祖鸟烯的一氯代物有4种
D.始祖鸟烯既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,则两反应的反应类型是相同的
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

(1)电源B极的名称是________。
(2)如果收集乙装置中两极产生的气体,两极气体的物质的量之比是________。
(3)甲装置中电解反应的总化学方程式:_______________________。
(4)欲用丙装置给铁镀锌,G应该是_______(填“铁”或“锌”),电镀液的主要成分是_______(填化学式)。
(5)装置丁中的现象是___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们经常食用的牛、羊、猪等肉类和白菜、土豆等蔬菜,经消化吸收后,其中的成分可被转化为人体的组成成分。对以上事实解释合理的是
A. 组成生物体细胞的化学元素在无机自然界都能找到
B. 不同生物的细胞内,组成它们的化学元素含量大体相同
C. 组成生物体细胞的生物大分子都是以碳链作为骨架
D. 不同生物的细胞内,组成它们的化学元素种类大体相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达正确的是
A.向Al2(SO4)3溶液中加入过量氨水:Al3++4NH3·H2O==AlO2-+4NH4++2H2O
B.向漂白粉稀溶液中通入过量CO2:ClO-+CO2+H2O==HClO+HCO![]()
C.向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO![]() 完全沉淀:
完全沉淀:
NH4++Al3++SO42-+Ba2++4OH-==NH3·H2O+Al(OH)3↓+BaSO4↓
D.酸性溶液中KIO3与KI反应:I-+IO3-+6H+==I2+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法不利于“开源节流”的是
A. 开发太阳能、水能、风能、地热能等新能源
B. 大力开采煤、石油和天然气,以满足人们日益增长的能源需求
C. 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D. 减少资源消耗,注重资源的重复使用、资源的循环再生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:

生成氢氧化物沉淀的pH:
Mg(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 9.4 | 6.3 | 1.5 |
完全沉淀时 | 12.4 | 8.3 | 2.8 |
(1)MgCO3 与稀硫酸反应的离子方程式为_______________________。
(2)加双氧水的目的______________________;相关的离子方程式_________________________;加氨水调节溶液的PH范围为______________。
(3)滤渣2 的成分是_____________(填化学式)。
(4)煅烧过程存在以下反应:2MgSO4+C![]() 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C![]() MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C![]() MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。
①D中收集的气体可以是________________(填化学式)。
②B中盛放的溶液可以是________________(填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为3 L的密闭容器中反应CO(g)+ 2H2(g)![]() CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。
(1)反应的平衡常数表达式K=_____________;根据下图,升高温度,K值将__________(填“增大”、“减小”或“不变”)。
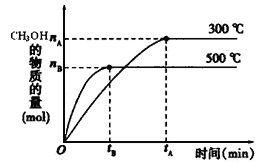
(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是__________(用nB、tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是____________ (填字母)。
a.v生成(CH3OH)= v消耗(CO)
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是(填字母)___________________。
a.c(H2)减少 b.正反应速率加快,逆反应速率减慢
c.CH3OH 的物质的量增加 d.重新平衡时c(H2)/ c(CH3OH)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关组成生物体的化学元素的叙述,不正确的是( )
A. 碳是构成细胞的最基本元素(占细胞干重百分比最多)
B. C、H、O、N、P、S、K、Ca、Mg都是大量元素
C. 组成生物体的化学元素在无机自然界都可以找到
D. 微量元素含量很少,因此作用很小,可有可无
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电化学装置的叙述正确的是 ( )

A. 图1中,Zn—MnO2干电池放电时,MnO2被氧化
B. 图2中,电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等
C. 图4中,在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl7-形式存在,则阳极反应式为:Al -3e-+7AlCl4-=4Al2Cl7-
D. 图3中,K分别与M、N连接,均可保护Fe电极,连接M时称为“牺牲阳极的阴极保护法”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com