
| ŃōĄė×Ó | K+”¢Ag+”¢Mg2+”¢Ba2+ |
| ŅõĄė×Ó | NO3-”¢CO32-”¢SiO32-”¢SO42- |
| A£® | K+Ņ»¶Ø“ęŌŚ£¬ĒŅc£ØK+£©”Ü1.3mol•L-1 | |
| B£® | ŹµŃéIÄÜČ·¶ØŅ»¶Ø²»“ęŌŚµÄĄė×ÓŹĒAg+”¢Mg2+”¢Ba2+ | |
| C£® | ŹµŃéIÖŠÉś³É³ĮµķµÄĄė×Ó·½³ĢŹ½ĪŖSiO32-+2H+=H2SiO3”ż | |
| D£® | ŹµŃéIIIÄÜČ·¶ØŅ»¶Ø²»“ęŌŚSO42- |
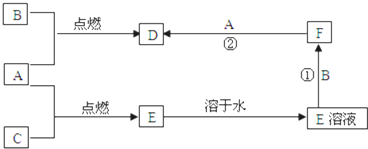
·ÖĪö I£®ĻņøĆČÜŅŗÖŠ¼ÓČė×ćĮæĻ”HCl£¬²śÉś°×É«³Įµķ²¢·Å³ö1.12LĘųĢ壬ĘųĢåĪŖ¶žŃõ»ÆĢ¼£¬ŌņŅ»¶Øŗ¬CO32-£¬Ōņ²»ŗ¬Ag+”¢Mg2+”¢Ba2+£¬n£ØCO32-£©=n£ØCO2£©=1.12L”Ā22.4L/mol=0.05mol£»
II£®½«IµÄ·“Ó¦»ģŗĻŅŗ¹żĀĖ£¬¶Ō³ĮµķĻ“µÓ”¢×ĘÉÕÖĮŗćÖŲ£¬³ĘµĆ¹ĢĢåÖŹĮæĪŖ3.6g£¬æÉÖŖIÖŠ°×É«³Įµķŗ¬¹čĖį£¬ŌņŌČÜŅŗŅ»¶Øŗ¬SiO32-£¬n£ØSiO32-£©=n£ØSiO2£©=3.6g”Ā60g/mol=0.06mol£»
III£®ŌŚIIµÄĀĖŅŗÖŠµĪ¼ÓBaCl2ČÜŅŗ£¬ĪŽĆ÷ĻŌĻÖĻó£¬æÉÖŖŌČÜŅŗŅ»¶Ø²»ŗ¬SO42-£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗI£®ĻņøĆČÜŅŗÖŠ¼ÓČė×ćĮæĻ”HCl£¬²śÉś°×É«³Įµķ²¢·Å³ö1.12LĘųĢ壬ĘųĢåĪŖ¶žŃõ»ÆĢ¼£¬ŌņŅ»¶Øŗ¬CO32-£¬Ōņ²»ŗ¬Ag+”¢Mg2+”¢Ba2+£¬n£ØCO32-£©=n£ØCO2£©=1.12L”Ā22.4L/mol=0.05mol£»
II£®½«IµÄ·“Ó¦»ģŗĻŅŗ¹żĀĖ£¬¶Ō³ĮµķĻ“µÓ”¢×ĘÉÕÖĮŗćÖŲ£¬³ĘµĆ¹ĢĢåÖŹĮæĪŖ3.6g£¬æÉÖŖIÖŠ°×É«³Įµķŗ¬¹čĖį£¬ŌņŌČÜŅŗŅ»¶Øŗ¬SiO32-£¬n£ØSiO32-£©=n£ØSiO2£©=3.6g”Ā60g/mol=0.06mol£»
III£®ŌŚIIµÄĀĖŅŗÖŠµĪ¼ÓBaCl2ČÜŅŗ£¬ĪŽĆ÷ĻŌĻÖĻó£¬æÉÖŖŌČÜŅŗŅ»¶Ø²»ŗ¬SO42-£¬
ÓɵēŗÉŹŲŗćæÉÖŖ£¬ŅõĄė×ÓµēŗÉ×ÜŹż“óÓŚŃōĄė×ÓµēŗÉ×ÜŹż£¬ŌņŌČÜŅŗŅ»¶Øŗ¬K+£¬
×ŪÉĻĖłŹö£¬ŌČÜŅŗŅ»¶Øŗ¬K+”¢Na+”¢CO32-”¢SiO32-£¬²»ŗ¬Ag+”¢Mg2+”¢Ba2+”¢SO42-£¬æÉÄÜŗ¬NO3-£¬
A£®K+Ņ»¶Ø“ęŌŚ£¬Čō²»ŗ¬NO3-£¬ÓɵēŗÉŹŲŗćæÉÖŖ£¬0.5mol/L”Į2+0.6mol/L”Į2=0.9mol/L+c£ØK+£©£¬Ōņc£ØK+£©”Ż1.3mol•L-1£¬¹ŹA“ķĪó£»
B£®ŹµŃéIŅ»¶Øŗ¬CO32-£¬ÄÜČ·¶ØŅ»¶Ø²»“ęŌŚµÄĄė×ÓŹĒAg+”¢Mg2+”¢Ba2+£¬¹ŹBÕżČ·£»
C£®¢ņÖŠæÉÄܳĮµķ¼ÓČČ·Ö½ā£¬ŌņŹµŃéIÖŠÉś³É³ĮµķµÄĄė×Ó·½³ĢŹ½ĪŖSiO32-+2H+=H2SiO3”ż£¬¹ŹCÕżČ·£»
D£®ŹµŃéIIIÄÜČ·¶Ø²»Éś³ÉĮņĖį±µ³Įµķ£¬ŌņŅ»¶Ø²»“ęŌŚSO42-£¬¹ŹDÕżČ·£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļµÄĶʶĻ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ·¢ÉśµÄĄė×Ó·“Ó¦”¢ĻÖĻ󔢵ēŗÉŹŲŗćĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėĶʶĻÄÜĮ¦µÄ漲飬עŅā°×É«³Įµķ¼°ĘųĢåµÄÅŠ¶Ļ£¬ĢāÄæÄŃ¶Č²»“ó£®


 æģ½ŻÓ¢ÓļÖÜÖÜĮ·ĻµĮŠ“š°ø
æģ½ŻÓ¢ÓļÖÜÖÜĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO32-Ąė×ÓŹĒČõĖįøł£¬æŖŹ¼½×¶ĪÓėH+½įŗĻ£¬Éś³ÉHCO3- | |
| B£® | ČÜŅŗÖŠµÄNa+”¢Cl-ŅÖÖĘĮĖCO2Éś³É | |
| C£® | æŖŹ¼Éś³ÉµÄCO2ÓėNa2CO3·“Ó¦£¬Éś³ÉĮĖNaHCO3 | |
| D£® | CO32-Ąė×ÓŌŚĖ®ÖŠ£¬“ęŌŚĮ½øöĖ®½āĘ½ŗā£¬æŖŹ¼½×¶ĪæÉÄÜŹĒH+½įŗĻOH-£¬Éś³ÉHCO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ĪļÖŹ | ŌÓÖŹ | ŹŌ¼Į | Ģį“æ·½·Ø | |
| A | ±½ | ±½·Ó | äåĖ® | ·ÖŅŗ |
| B | ¶žŃõ»ÆĢ¼ | ¶žŃõ»ÆĮņ | ±„ŗĶĢ¼ĖįÄĘČÜŅŗ | Ļ“Ęų |
| C | ¼×Ķé | ŅŅĻ© | ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ | Ļ“Ęų |
| D | ¼×Č© | ¼×Ėį | Ļ”ĒāŃõ»ÆÄĘČÜŅŗ | ÕōĮó |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ¼×ŌŚ¹āÕÕĢõ¼žĻĀÓėCl2·“Ó¦æɵƵ½ĖÄÖÖ²»Ķ¬µÄ²śĪļ | |
| B£® | ŅŅ”¢±ūĖłÓŠµÄŌ×Ó¾ł“¦ÓŚĶ¬Ņ»Ę½Ćę£¬¾łæÉŹ¹äåĖ®·“Ó¦ĶŹÉ« | |
| C£® | ŹÆÓĶ·ÖĮóæÉ»ńµĆ¼×ŗĶŅŅ£¬ĆŗøÉĮóæÉ»ńµĆ±ū | |
| D£® | ŌŚÅØĮņĖį“ęŌŚĻĀ£¬±ūÓėÅØĻõĖį¹²Čȵķ“Ó¦ŹōÓŚČ”“ś·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 8£¬18£¬32£¬32 | B£® | 8£¬18£¬18£¬32 | C£® | 8£¬18£¬18£¬18 | D£® | 8£¬8£¬18£¬18 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5.6 g ĢśŌŚ×ćĮæĀČĘųÖŠČ¼ÉÕ£¬µē×Ó×ŖŅĘ0.2 NAøö | |
| B£® | 7.8 gµÄNa2O2Óė×ćĮæµÄĖ®·“Ó¦ŗóČÜŅŗµÄĢå»żĪŖ1L£¬øĆČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ0.2mol/L | |
| C£® | 1.12 LĀČĘųÖŠŗ¬ÓŠ0.1 NAøöĀČŌ×Ó | |
| D£® | ±ź×¼×“æöĻĀ£¬2.24 LSO3ÖŠŗ¬ÓŠ0.3NAøöŃõŌ×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶£ŗNa£¾P£¾O£¾F | B£® | ĪČ¶ØŠŌ£ŗPH3£¼NH3£¼H2O£¼HF | ||
| C£® | ¼īŠŌ£ŗKOH£¾NaOH£¾Mg£ØOH£©2 | D£® | »¹ŌŠŌ£ŗF-£¾Cl-£¾Br- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com