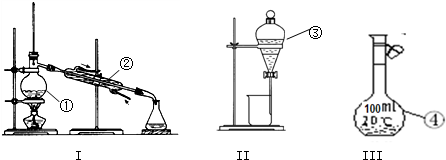
考点:溶液的配制,物质的分离、提纯和除杂,物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题,计算题
分析:(1)根据配置一定物质的量浓度的溶液所需操作步骤和每一步操作所需仪器分析;
(2)除去KCl溶液中的SO42-,应使SO42-离子转化为沉淀,注意不能引入新的杂质;
(3)检验滤液中是否存在SO42-离子.
解答:
解:(1)配制一定物质的量的浓度的溶液需要称量、溶解、洗涤、移液、定容等操作,溶解需要烧杯、玻璃棒,定容需要胶头滴管、需要100mL容量瓶进行配制,故答案为:烧杯,玻璃棒,100 mL容量瓶 胶头滴管;
(2)除去KCl溶液中的SO42-,应先加入过量BaCl2使SO42-生成沉淀,然后加入K2CO3使过量的BaCl2生成沉淀,过滤后加入HCl除去过量的K2CO3,
故答案为:BaCl2、K2CO3、HCl;
(3)检验滤液中是否存在SO42-离子,用氯化钡通过生成硫酸钡来检验,具体操作为:取所得溶液的上层清液1~2滴于滴定板上,再滴入1-2滴BaCl2溶液,若溶液未变浑浊,则表明SO42-已沉淀完全.
故答案为:取所得溶液的上层清液1~2滴于滴定板上,再滴入1-2滴BaCl2溶液,若溶液未变浑浊,则表明SO42-已沉淀完全.
点评:本题考查物质的分离、提纯的基本方法选择与应用,题目难度中等,注意根据混合物组分性质的差异性选择分离的方法,本题易错点为(2),注意加入试剂的顺序和除杂原理.



 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案