
| A. | SiO2 | B. | Na2O | C. | Na2O2 | D. | NaOH |
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题
| A. | 神舟九号升空时火箭发射的动力主要来源于化学能 | |
| B. | 洁厕灵的主要成分是盐酸,不能与“84”消毒液混用 | |
| C. | 采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 | |
| D. | 高纯硅广泛应用于太阳能电池、计算机芯片和光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
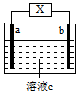
| A. | a、b不可能是同种材料的电极 | |
| B. | X为电流计,c为稀盐酸,该装置为原电池 | |
| C. | X为直流电源,c为稀硫酸,该装置为电解池 | |
| D. | X为电流计,c为稀硫酸,a可能为铜电极,b可能为锌电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.0×10-7 mol•L-1 | B. | 1.0×10-7 mol•L-1 | ||
| C. | 1.0×10-14/5.0×10-7 mol•L-1 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 | |
| B. | 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 | |
| C. | 反应CO(g)+NO2 (g)?CO2 (g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 | |
| D. | 对于2HI(g)?H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.lmol Fe在0.lmolCl2中充分燃烧,转移的电子数为0.3NA | |
| B. | 25℃时,pH=13的1.0 LBa(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 含NA个氧原子的O2与含NA个氧原子的O3的质量比为2:3 | |
| D. | lmol CnH2n+2分子中含共价键数目为(3n+1)NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子的最外层电子数都是7,次外层电子数都是8 | |
| B. | 单质的化学性质活泼,易得电子发生还原反应 | |
| C. | 单质都有颜色,且颜色逐渐变浅 | |
| D. | 都难溶于水,且不与水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuCl2[CuCl2] | B. | NaOH[H2O] | C. | NaCl[HCl] | D. | CuSO4[Cu(OH)2] |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com