


 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(a) | B、(b) |
| C、(a)(c) | D、(a)(d) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水溶解,观察溶液温度变化 |
| B、取相同质量敞口放置,过一段时间在称量,比较质量变化 |
| C、取相同量,加入到氯化钡溶液中,观察是否有沉淀产生 |
| D、取相同量于试管中,加入铜片,加热观察,是否有刺激性气味的气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |
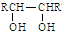
| △H2SO4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| ① |
| 过量稀硫酸 |
| ②操作a |
| ③双氧水 |
| H+ |
| ④氨水 |
| 操作b |
| ⑤灼烧 |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取NaCl固体29.25g |
| B、应选用500 mL的容量瓶来配制此溶液 |
| C、在转移操作中不慎将溶液洒到容量瓶外面,应该重新配置溶液 |
| D、加蒸馏水至离刻度线1-2 cm时改用胶头滴管定容 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com