
Li��SOCl2��ؿ����������������õ�صĵ缫���Ϸֱ�Ϊ﮺�̼�����Һ��LiAlCl4��SOCl2����ص��ܷ�Ӧ�ɱ�ʾΪ��4Li+2SOCl2=4LiCl+S+SO2��
��1��������������ĵ缫��ӦΪ����
��2��SOCl2�ӷ���ʵ�����г���NaOH��Һ����SOCl2����Na2SO3��NaCl���ɣ� ���������ˮ�ε�SOCl2�У�ʵ��������������Ӧ�Ļ�ѧ����ʽΪ����
| ԭ��غ͵��صĹ���ԭ����. | |
| ������ | ���ܷ�Ӧ��֪����ԭ�����Li��������ӦΪԭ��ظ�����Ӧ���缫��ӦʽΪLi��e��=Li+��SOCl2�������õ��ӱ���ԭ����S���缫��ӦΪ2SOCl2+4e��=4Cl��+S+SO2���õ�ر�������ˮ�������������½��У������H2O��O2��Ӧ��SOCl2Ҳ����ˮ��Ӧ�� |
| ��� | �⣺��1��SOCl2�������õ��ӱ���ԭ����S��ͬʱ������SO2���缫��ӦΪ2SOCl2+4e��=4Cl��+S+SO2�� �ʴ�Ϊ��2SOCl2+4e��=4Cl��+S+SO2�� ��2��ʵ�����г���NaOH��Һ����SOCl2����Na2SO3��NaCl���ɣ���֪SOCl2��ˮ��Ӧ����SO2��HCl����Ӧ�ķ���ʽΪ SOCl2+H2O=SO2��+2HCl��������������д̼��Բ��γ������� �ʴ�Ϊ�����ְ������д̼����������ɣ�SOCl2+H2O=SO2��+2HCl���� |
| ������ | ���⿼��Li��SOCl2��ص���ɺ���ԭ������Ŀ�Ѷ��еȣ��ӵ���ܷ�Ӧʽ�жϵ缫��Ӧ���Լ��缫����ʽ����д�Ǹò��ֳ����鷽ʽ��ϣ��ѧϰ�ж�ע��������֪ʶ�ͽ���� |
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijʵ��С����H2O2�ֽ�Ϊ�����о�Ũ�ȡ���������Һ����ԶԷ�Ӧ���ʵ�Ӱ�졣�ڳ����°������·������ʵ�顣
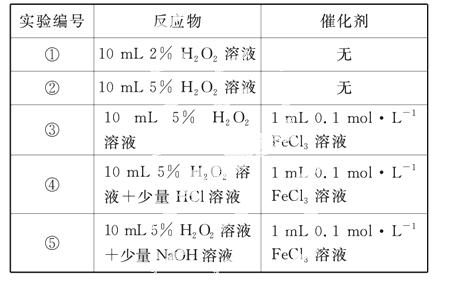
(1)�����ܼӿ컯ѧ��Ӧ���ʵ�ԭ����____________��
(2)ʵ��ٺ͢ڵ�Ŀ����___________________��
ʵ��ʱ����û�й۲쵽������������ó����ۡ�������ʾ��ͨ��������H2O2�ȶ������ֽ⡣Ϊ�˴ﵽʵ��Ŀ�ģ����ԭʵ�鷽���ĸĽ���__________��
(3)ʵ��ۡ��ܡ����У�������������������ʱ��仯�Ĺ�ϵ����ͼ��
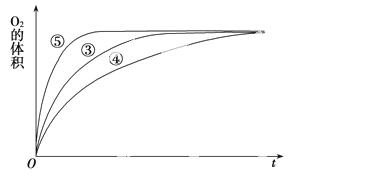
������ͼ�ܹ��ó���ʵ�������____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ�����ӵ�������ֵ������˵������ȷ����
A�����³�ѹ�£�2.3 g Na���Na2O2ʱ��ʧȥ0.2NA������
B�����³�ѹ�£�32 g������32 g����������2NA����ԭ��
C��500 mL 0.2 mol/L NaOH��Һ�к���NA��Na+����
D����20�桢1.01��105Paʱ��11.2 L��������NA����ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������Ϊ100g��Cu���缫�����AgNO3��Һ���Ե��һ��ʱ������缫���������28g����ʱ���缫�������ֱ�Ϊ��������
| �� | A�� | ����100 g������128 g | B�� | ����93.6 g������121.6 g |
| �� | C�� | ����91.0 g������119.0 g | D�� | ����86.0 g������114.0 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л�ѧ��Ӧ�����ӷ���ʽ��ȷ���ǣ�������
| �� | A�� | ��������Һ����μ�������������Һ��SO42��ǡ����ȫ����Al3++2 SO42��+2 Ba2++4 OH��=2 BaSO4��+AlO2��+2 H2O |
| �� | B�� | ����SO2ͨ��Ca��ClO��2��Һ�У�SO2+H2O+Ca2++2ClO��=CaSO3��+2HClO |
| �� | C�� | ��ϡHNO3��Һ�ܽ�FeS���壺FeS+2H+=Fe2++H2S�� |
| �� | D�� | AgNO3��Һ�м�������İ�ˮ��Ag++NH3•H2O=AgOH��+NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӣ����ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ���⣮
��1������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�ӦCO��g��+H2O��g��⇌CO2��g��+H2��g���õ������������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/nin |
| |
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
��ʵ��1�ӿ�ʼ���ﵽ��ѧƽ��ʱ����v��CO2����ʾ�ķ�Ӧ����Ϊ����������ȷ��0.01����ͬ��
�ڸ÷�ӦΪ������������š����ȷ�Ӧ��ʵ��2������ƽ�ⳣ��K=������
��2���Զ����ѣ�CH3OCH3������������������Ϊԭ�ϣ���Ϊ�缫�ɹ���ȼ�ϵ�أ��乤��ԭ�� �����ȼ�ϵ�ص�ԭ�����ƣ���д���õ�ظ����ϵĵ缫��Ӧʽ��������
��3����֪H2��g����CO��g����CH3OH��l����ȼ���ȷֱ�Ϊ��285.8kJ•mol��1����283.0kJ•mol ��1�ͩ�726.5kJ•mol��1����д���״���CH3OH������ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ʰ��ᡢ��η���˳��������ȷ���ǣ�������
| �� | A�� | ���ᡢ���ʯ�� | B�� | �����ᡢ�ռ�̷� |
| �� | C�� | ���ᡢ�Ҵ��������� | D�� | ���ᡢ��ʯ�ҡ����Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
x g H2O�к���y����ԭ�ӣ����ӵ�����Ϊ�� ��
A��9x/y mol-1 B��9y/x mol-1 C��x/y mol-1 D��y/x mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����200ml0.1mol/Lϡ������Һʱ������ʵ�����ʹ��������ҺŨ��ƫС���ǣ� ��
A�����ݺ�ҡ�ȣ�����Һ����͵���ڿ̶��ߣ��ٲ��Ӽ�������ˮ���̶���
B������Ͳ��ȡ�����Ũ����ʱ���Ӷ���
C������ʱ�����ӿ̶���
D������Ͳ��ȡŨ���ᵹ���ձ�����������ˮϴ��Ͳ2~3�Σ�ϴҺ�����ձ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com