
| A. | 硫酸、烧碱、醋酸钠、AlO2•2SiO2•2H2O分别属于酸、碱、盐和氧化物 | |
| B. | 蔗糖、硝酸钾和硫酸钡分别属于非电解质、强电解质和弱电解质 | |
| C. | CuSO4•5H2O、冰醋酸、冰水混合物属于纯净物;水玻璃、氢氧化铁胶体属于混合物 | |
| D. | SO2、SiO2、CO属于酸性氧化物;CuO、Fe2O3、Na2O2属于碱性氧化物 |
分析 A、AlO2•2SiO2•2H2O是硅酸盐;
B、在水溶液中能完全电离的化合物为强电解质,不能完全电离的为弱电解质;
C、只由一种物质构成的是纯净物;由两种或以上物质构成的是混合物;
D、能和碱反应生成盐和水的氧化物为酸性氧化物;能和酸反应生成盐和水的氧化物为碱性氧化物.
解答 解:A、硫酸是酸;烧碱即NaOH,是碱;醋酸钠是盐;AlO2•2SiO2•2H2O是硅酸盐的氧化物的形式,而不是氧化物,故A错误;
B、在水溶液中能完全电离的化合物为强电解质,不能完全电离的为弱电解质,硫酸钡虽然难溶于水,但在水溶液中能完全电离,故为强电解质,故B错误;
C、只由一种物质构成的是纯净物,故CuSO4•5H2O、冰醋酸、冰水混合物属于纯净物;由两种或以上物质构成的是混合物,而水玻璃是硅酸钠的水溶液,是混合物;胶体属于分散系,也是混合物,故C正确;
D、能和碱反应生成盐和水的氧化物为酸性氧化物,故CO不是酸性氧化物;能和酸反应生成盐和水的氧化物为碱性氧化物,故过氧化钠不是碱性氧化物,故D错误.
故选C.
点评 本题考查了化学中的常见的概念和物质的分类,掌握概念的要点是解题的关键,应注意的是强弱电解质的本质区别是能否完全电离,和溶解度无关.


科目:高中化学 来源: 题型:选择题
| A. | CO2不能与KNO3溶液反应,推测SO2也不能与KNO3溶液反应 | |
| B. | 由“2Fe+3Cl2=2FeCl3”反应可推出“2Fe+3Br2=2FeBr3”反应也能发生 | |
| C. | 由氢氟酸刻蚀玻璃可推知盐酸也能用来刻蚀玻璃 | |
| D. | Zn(OH)2能与氨水反应,则Al(OH)3也能与氨水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 配料表 | 精制海盐、碘酸钾(KIO3) |
| 含碘盐 | 20~40mg/kg |
| 储藏方法 | 密封避光、防潮 |
| 使用方法 | 烹调时待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度(mol•L-1) | 0.44 | 0.6 | 0.6 |
| A. | a=1.64 | |
| B. | 此时刻正反应速率大于逆反应速率 | |
| C. | 0-10min内平均反应速率v(CH3OH)=1.6 mol/(L•min) | |
| D. | 若混合气体的平均摩尔质量不再变化,则说明反应已达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为34,质子数为29的铜原子:${\;}_{34}^{63}$Cu | |
| B. | 碳原子的结构示意图: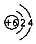 | |
| C. | 二氧化碳的电子式: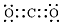 | |
| D. | 乙醇的结构简式:CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸铵自发地溶于水 | |
| B. | H2O(l)═H2O(g)△H=+44.0kJ•mol-1 | |
| C. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9 kJ•mol-1 | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量NaOH固体时动作缓慢 | B. | 定容时俯视刻度线 | ||
| C. | 定容后振荡发现液面低于刻度线 | D. | 未洗涤烧杯和玻璃棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol C3H8气体中含有共价键数目为11NA | |
| B. | 1mol Na2O和Na2O2混合物中含有的阴阳离子总数是3NA | |
| C. | 将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA个Fe3+ | |
| D. | 标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com