
【题目】常温时,下列叙述正确的是![]()
A.![]() 的
的![]() 与
与![]() 混合溶液中
混合溶液中![]()
B.![]() 的可乐中
的可乐中![]() 是
是![]() 的柠檬水中
的柠檬水中![]() 的10倍
的10倍
C.AgCl在![]()
![]() 溶液和
溶液和![]() NaCl溶液中的溶解度相同
NaCl溶液中的溶解度相同
D.![]() 溶液加水稀释至100mL,pH和
溶液加水稀释至100mL,pH和![]() 均减小
均减小
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】某化工厂每小时生产a 吨98%(质量分数)硫酸。为使硫充分燃烧,且在下一步催化氧化时不再补充空气,要求燃烧后的混合气体中含氧气的体积分数为b%。若空气中氧气的体积分数为21%,且不考虑各生产阶段的物料损失,则
(1)该厂每小时消耗标准状况下空气的体积为___________m3。
(2)为满足题设要求,b%的下限等于___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C时,c(CH3COOH)+ c(CH3COO-)=0.1mol/L的醋酸、醋酸钠混合溶液中,c(CH3COOH)、 c(CH3COO-)与pH的关系如图所示。下列有关该溶液的叙述不正确的是
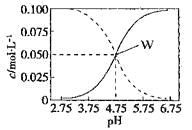
A.pH=4的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.W点所表示的溶液中:c(Na+)+ c(H+)= c(CH3COOH)+c(OH-)
C.将W点所表示的1.0L溶液稀释到10L,用pH计测量,溶液的pH应为5.75
D.pH=5.5的溶液中:c(Na+)+ c(H+)- c(OH-)+c(CH3COOH)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________,B是________,E是_________。(请填写元素符号)
(2) 写出C元素基态原子的电子排布式_________________________。
(3) 用轨道表示式表示D元素原子的最外层电子构型____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究某溶液中溶质R的分解速率的影响因素,分别用三份不同初始浓度的R溶液在不同温度下进行实验,c(R)随时间变化如图。下列说法不正确的是( )

A. 25 ℃时,在0~30 min内,R的分解平均速度为0.033 mol·L-1·min-1
B. 对比30 ℃和10 ℃曲线,在50 min时,R的分解百分率相等
C. 对比30 ℃和25 ℃曲线,在0~50 min内,能说明R的分解平均速度随温度升高而增大
D. 对比30 ℃和10 ℃曲线,在同一时刻,能说明R的分解速率随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B. 图乙表示向CH3COOH溶液中加水时溶液的导电性变化,且CH3COOH溶液的pH:a>b
C. 图丙表示加入催化剂,化学反应的焓变减小
D. 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) ![]() N2O4(g),相同时间后测得NO2含量的曲线,则该反应的H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积不变的密闭容器中,保持一定的温度发生下列反应:4A(g)+B(?)2C(g)+2D(g),请用“增大”“减小”“不变”或“能”“不能”填空。
(1)当B为固体时,若反应向右进行,容器内混合气体的密度___________;若反应向左进行,容器内混合气体的密度___________;当容器内混合气体的密度不变时___________说明反应已经达到平衡。
(2)当B为气体时,不论向哪个方向反应,容器内混合气体的密度___________,故当容器内混合气体的密度不变时___________说明反应已经达到平衡。
(3)当B为固体时,无论向哪个方向反应,容器内混合气体的压强___________,故当容器内混合气体的压强不变时___________说明反应已经达到平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.0 g铜与250 mL一定浓度的硝酸恰好完全反应,产生的NO和NO2混合气体在标准状况下的体积为11.2 L。(假定反应前后溶液体积不变,也不考虑N2O4的存在。)
试计算:
(1)硝酸的物质的量浓度是____________ molL-1
(2)若要使此混合气体被水完全吸收,需要通入标准状况下__________L O2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com