
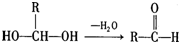 ����ش��������⣺
����ش��������⣺
 ��
�� ����
���� ��
��
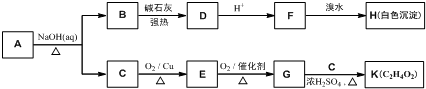
���� A����ˮ�ⷴӦC��D��E��C������D������������Ϣ��֪��C�Ľṹ��ʽΪCH3CHO��DΪCH3COONa��EΪNaBr��B������ʺɱ�Ϊ208������B����Է�������Ϊ208�����������ʾB�����к��б����ṹ�������������˴Ź�����������������շ壬���ֵ��Ϊ2��2��2��3��3�����б����ϵ�һ�ȴ���ֻ�����֣�B����ˮ���D��G��F��G���������õ�D����GΪCH3CH2OH������֪BΪ ��B����ˮ���FΪ
��B����ˮ���FΪ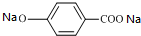 ��
��
��5��GΪCH3CH2OH����CH3CH2OHΪԭ�Ϻϳ���������������CH3COCH2COOC2H5�������������Ҵ����������ᣬ�Ҵ����Ҵ����������������������������Ƶ������·���������Ϣ�еķ�Ӧ����������������
��� �⣺A����ˮ�ⷴӦC��D��E��C������D������������Ϣ��֪��C�Ľṹ��ʽΪCH3CHO��DΪCH3COONa��EΪNaBr��B������ʺɱ�Ϊ208������B����Է�������Ϊ208�����������ʾB�����к��б����ṹ�������������˴Ź�����������������շ壬���ֵ��Ϊ2��2��2��3��3�����б����ϵ�һ�ȴ���ֻ�����֣�B����ˮ���D��G��F��G���������õ�D����GΪCH3CH2OH������֪BΪ ��B����ˮ���FΪ
��B����ˮ���FΪ ��
��
��1������A�Ľṹ��ʽ��֪��A�����������ŵ�����Ϊ��������ԭ�ӣ�
�ʴ�Ϊ����������ԭ�ӣ�
��2����������ķ�����֪��B�Ľṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��3����Ӧ�ٵķ���ʽΪ ��
��
��Ӧ �ܵķ���ʽΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
��4��BΪ ����ͬ���칹����ϣ������ڷ����廯���˵���б������ں�������ȡ����������ֻ��һ��������������ȡ������ͬ�Ҵ�������λ�ã����ܷ���ˮ�ⷴӦ��������Ӧ��˵����������ȩ���������������B��ͬ���칹��Ϊ�ڱ����ļ�λ��������-OOCH��һ��-C3H7�����������з�������-C3H7��2�ֽṹ�����Թ���6�ֽṹ��Ҳ�������ڱ����ļ�λ��������HCOOCH2-��һ��-CH3�����������з��������Թ���9�֣�
����ͬ���칹����ϣ������ڷ����廯���˵���б������ں�������ȡ����������ֻ��һ��������������ȡ������ͬ�Ҵ�������λ�ã����ܷ���ˮ�ⷴӦ��������Ӧ��˵����������ȩ���������������B��ͬ���칹��Ϊ�ڱ����ļ�λ��������-OOCH��һ��-C3H7�����������з�������-C3H7��2�ֽṹ�����Թ���6�ֽṹ��Ҳ�������ڱ����ļ�λ��������HCOOCH2-��һ��-CH3�����������з��������Թ���9�֣�
�ʴ�Ϊ��9��
��5����CH3CH2OHΪԭ�Ϻϳ���������������CH3COCH2COOC2H5�������������Ҵ����������ᣬ�Ҵ����Ҵ����������������������������Ƶ������·���������Ϣ�еķ�Ӧ�����������������ϳ�·��Ϊ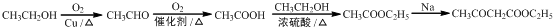 ��
��
�ʴ�Ϊ��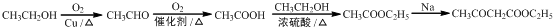 ��
��
���� ���⿼���л����ƶ���ϳɣ����ؿ���ѧ�������ƶ�������ȷ��B�Ľṹ��ʽ�ǽⱾ��ؼ��������л���Ĺ����ŵı仯Ϊͻ�ƿڽ����ƶϣ���Ҫѧ���������չ����ŵĽṹ�����ʣ��ѵ���ͬ���칹�������жϣ�


 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ�����л�ѧ����Ũ���ᣬ���Լ�ƿ��ǩ�ϵIJ���������ͼ��
ʵ�����л�ѧ����Ũ���ᣬ���Լ�ƿ��ǩ�ϵIJ���������ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ������ȡ�����������װ����ͼ��ʾ�������������������գ�
ʵ������ȡ�����������װ����ͼ��ʾ�������������������գ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������۵�ߣ�Ӳ�ȴ�����ˮ�ࡢ�մ��� | |
| B�� | ���������������쾧��ܡ����ɵ�· | |
| C�� | ����������������ʯӢ�ӱ���ѹ����Ϻ��ά | |
| D�� | ������������������������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �ݡ����� | �� | �� |
| ��Ӧ��Ͷ���� | 1mol CO2��3mol H2 | a��mol CO2��3a��mol H2�� b��mol CH3OH��g����b��mol H2O��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������������β���Ĵ�����������������߿������� | |
| B�� | ���ٻ�ʯȼ�ϵ�ʹ�ã������ڽ��Ϳ�����PM2.5�ĺ��� | |
| C�� | ʳƷ��װ���г�����С������ʯ�ң�Ŀ���Ƿ�ֹʳƷ�������� | |
| D�� | ҽ�þƾ����õ�����ֲ��;������Ƴɣ�Ũ��ͨ����75% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

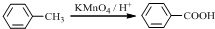
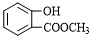 ��
��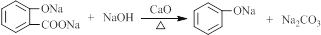 ��
��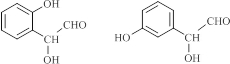 ��д�ṹ��ʽ����
��д�ṹ��ʽ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��úͨ�������仯Һ��������Ϊ��Դ���ɼ���PM2.5�����Σ�� | |
| B�� | ��������Ƭ��ά����Cͬʱ���ã�����ǿ����ȱ����ƶѪ��Ч�� | |
| C�� | ��ͨ�����������ǽ������ϣ��л����������������ǽ������� | |
| D�� | �������ǰ�ȫ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| 25�� | ����H2S��Һ | FeS | SnS | |
| pH | 3.9 | 3.0����ʼ���� | 5.5��������ȫ�� | 1.6��������ȫ�� |
| Ksp | 6.3��10-18 | 1.0��10-25 | ||
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com