
| A. | 由①可推测溶液中一定含大量CO32-、S2-、SO32-、NO3- | |
| B. | 由②可推测溶液中一定含大量NO2- | |
| C. | 由③可推测溶液中一定含大量NO3- | |
| D. | 由实验④难以推测溶液中一定含大量SO42- |
分析 ①取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,该黄色沉淀只能是S,将所得的气体依次通入品红溶液、品红褪色,气体含有SO2,通过足量酸性KMnO4溶液,除去SO2,再通过澄清石灰水,石灰水变浑浊,则气体为CO2,故原溶液含有CO32-、S2-、SO32-,酸性条件下S2-、SO32-反应生成S与SO2,不能说明溶液中含有氧化性的离子;
②另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生,该白色沉淀为AgCl,说明原溶液中含有还原性微粒,据此结合离子的性质分析判断;
③另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色,说明有碘单质生成,故原溶液中含有酸性条件有强氧化性的微粒;
④另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生,该白色沉淀为BaSO4,由于溶液中含有SO32-及酸性条件下有氧化性微粒,不能说明原溶液中含有SO42-.
解答 解:A.取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,该黄色沉淀只能是S,将所得的气体依次通入品红溶液、品红褪色,气体含有SO2,通过足量酸性KMnO4溶液,除去SO2,再通过澄清石灰水,石灰水变浑浊,则气体为CO2,故原溶液含有CO32-、S2-、SO32-,酸性条件下S2-、SO32-反应生成S与SO2,不能说明溶液中含有NO3-、NO2-,故A错误;
B.另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生,该白色沉淀为AgCl,说明原溶液中含有还原性微粒,由于原溶液有S2-、SO32-,不能说明溶液中含有NO2-,故B错误;
C.另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色,说明有碘单质生成,故原溶液中含有酸性条件有强氧化性的微粒,故原溶液中可能含有NO3-、NO2- 中的至少1种,故C错误;
D.另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生,该白色沉淀为BaSO4,由于溶液中含有SO32-及酸性条件下有氧化性微粒,可以将SO32-氧化为SO42-,不能说明原溶液中含有SO42-,故D正确;
故选D.
点评 本题考查离子检验与推断,注意干扰离子的影响,掌握离子之间发生的反应与现象是关键,难度中等.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  的名称为2,3-二甲基戊烷 的名称为2,3-二甲基戊烷 | |
| B. | 18.0g的葡萄糖与乳酸[CH3CH(OH)COOH]混合物完全燃烧消耗氧气13.44L | |
| C. | 结构片段为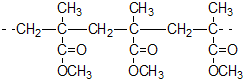 的高聚物,是通过加聚反应生成的 的高聚物,是通过加聚反应生成的 | |
| D. | 化合物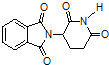 在氢氧化钠溶液中加热后有NH3生成 在氢氧化钠溶液中加热后有NH3生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在空气中,钢铁制品和铝制品都容易发生吸氧腐蚀 | |
| B. | 聚乙烯塑料易老化,是因为发生了加成反应 | |
| C. | 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 | |
| D. | 空气质量指标中有一项指标名称为PM2.5,指的是空气中直径≤2.5微米的固体或液体的总称 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com