
| A、该溶液中K2S的浓度为2mol?L-1 |
| B、C(K+)+C(H+)═C(HS-)+C(S2-)+C(OH-) |
| C、该溶液中水的电离程度大于常温下纯水的电离程度 |
| D、C(K+)>c(S2-)>C(HS-)>c(OH-)>C(H+) |
| v |
| vm |
| 4.48L |
| 22.4L/mol |
| n(KOH) |
| n(H2S) |
| 3 |
| 2 |
|
| v |
| vm |
| 4.48L |
| 22.4L/mol |
| n(KOH) |
| n(H2S) |
| 3 |
| 2 |
|
| n |
| v |
| 0.1mol |
| 0.1L |


科目:高中化学 来源: 题型:
| A、甲烷与氯气的混合气体在光照下生成的有机化合物均无同分异构体 |
| B、组成为C7H16的烷烃中仅能由一种单烯烃加氢而制得的有2种 |
C、某烃的结构简式可表示为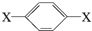 (碳原子数≤10).已知分子中有两种化学环境不同的氢原子,且数目之比为3:2,则该烃一定是苯的同系物 (碳原子数≤10).已知分子中有两种化学环境不同的氢原子,且数目之比为3:2,则该烃一定是苯的同系物 |
| D、含5个碳原子的有机物,每个分子中最多可形成4个C-C键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单位物质的量气体所占的体积就是气体摩尔体积 |
| B、气体的摩尔体积都相同 |
| C、H2O的摩尔质量是18g/mol |
| D、1mol Na+的质量是23 g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、C1-、HCO3-、K+ |
| B、Fe3+、OH-、Cl-、Na+ |
| C、Na+、NO3-、C1-、K+ |
| D、Ag+、NO3-、Cl-、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com