解答:
解:A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大,A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素,A为H元素;
B元素原子的核外p电子数比s电子数少1,B有2个电子层,为1s
22s
22p
3,故B为N元素;由C原子的第一至第四电离能数据可知,第三电离能剧增,故C表现+2价,处于ⅡA族,原子序数大于N元素,故C为Mg元素;D处于第三周期,D原子核外所有p轨道全满或半满,最外层排布为3s
23p
3,故D为P元素;E处于第三周期,E元素的主族序数与周期数的差为4,E处于第ⅦA族,故E为Cl元素;F是前四周期中电负性最小的元素,F为第四周期元素,故F为K元素,G在第四周期周期表的第7列,G为Mn元素;H元素原子价电子排布式为3d
104s
1,H为Cu元素.
(1)F为9号元素,核外电子数为9,基态原子的核外电子排布式为1S
22S
22P
5,PCl
3中P原子孤电子对数为1,成3个σ键,则为sp
3杂化,故答案为:1S
22S
22P
5;sp
3;
(2)BA
5为离子化合物,则为NH
4H,其电子式为
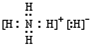
;
H、A、B三种元素会形成一种配合物的阳离子,其溶液显深蓝色,则为Cu离子溶于氨水形成Cu(NH
3)
42+溶液,其中配离子的结构简式为
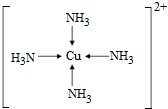
,
故答案为:
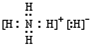
;
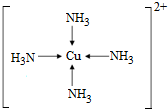
;
(3)根据F晶体的晶胞可知,为体心立方,晶胞中F原子数目=1+8×
=2,故晶胞质量=2×
g,若设该晶胞的密度为ag?cm
-3,则晶胞体积=
=
cm
3,则晶胞棱长=
cm,令F原子的半径为r cm,晶胞体对角线上的3个F原子相邻,则:(4r)
2=3(
)
2解得r=
,
故答案为:
;
(4)CuH和氯气反应生成氯化铜和氯化氢气体,6.5gCuH的物质的量为
=0.1mol,故该反应的热化学方程式为2CuH(s)+3Cl
2(g)=2CuCl
2 (s)+2HCl(g)△H=-20aKJ/mol;故答案为:2CuH(s)+3Cl
2(g)=2CuCl
2 (s)+2HCl(g)△H=-20aKJ/mol;
+1价的Cu被氧化为+2价,生成CuCl2
(5)将CMg
3N
2 加入HCl的水溶液中反应生成二种盐氯化镁和氯化铵,反应方程式为Mg
3N
2+8HCl=3MgCl
2+2NH
4Cl;
将浓度为a mol/LNH
3溶液和0.1mol?L
-1HCl溶液等体积混合后溶液呈中性,依据溶液中电荷守恒c(NH
4+)+c(H
+)=c(OH
-)+c(Cl
-),溶液呈中性说明c(H
+)=c(OH
-)=10
-7mol/L;c(NH
4+)=c(Cl
-)=0.005mol/L,则NH
3溶液的电离常数=
=
=
.
故答案为:.
.

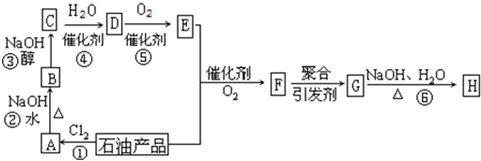
 现有8种元素,它们的原子序数依次增大,其中A、B、C、D、E为短周期主族元素,F、G、H为第四周期元素.请根据下列相关信息,回答问题.
现有8种元素,它们的原子序数依次增大,其中A、B、C、D、E为短周期主族元素,F、G、H为第四周期元素.请根据下列相关信息,回答问题.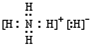 ;
; ,
,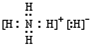 ;
; ;
;

 (1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是
(1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是

