
| A. | 原子半径W>X>Y | B. | W2Y的电子式为: | ||
| C. | 元素的金属性W<X | D. | W2Y2中既有离子键,又有共价键 |
分析 W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水,可知W为Na,X为Al,Y的最外层电子数是核外电子层数的2倍,应为S,结合对应单质、化合物的性质以及元素周期律知识解答该题.
解答 解:W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水,可知W为Na,X为Al,Y的最外层电子数是核外电子层数的2倍,应为S,
A.同周期元素从左到右原子半径逐渐减小,故A正确;
B.W2Y为Na2S,电子式为 ,故B正确;
,故B正确;
C.同周期元素从左到右金属性逐渐减弱,故C错误;
D.Na2O2中钠离子和过氧根离子之间存在离子键、O原子之间存在非极性共价键,故D正确.
故选C.
点评 本题考查原子结构与元素周期律的关系,侧重于物质的性质的递变规律的考查,根据原子结构明确元素的种类为解答该题的关键.


科目:高中化学 来源: 题型:选择题
 2010春节(虎年)的到来.农艺师对盆栽鲜花施用了S-诱抗素剂(分子结构如图),以使鲜花按时盛开.下列说法不正确的是( )
2010春节(虎年)的到来.农艺师对盆栽鲜花施用了S-诱抗素剂(分子结构如图),以使鲜花按时盛开.下列说法不正确的是( )| A. | S-诱抗素的分子式为C15 H20 O4 | |
| B. | S-诱抗素既能发生加聚反应,又能发生缩聚反应 | |
| C. | 1 mol S-诱抗素最多能和含1 mol NaOH的水溶液发生反应 | |
| D. | S-诱抗素既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
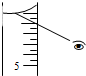 用18.4mol•L-1的浓H2SO4配制100mL浓度为1mol•L-1的稀H2SO4,其操作可分为以下各步:
用18.4mol•L-1的浓H2SO4配制100mL浓度为1mol•L-1的稀H2SO4,其操作可分为以下各步:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17g甲基(-14CH3)所含的中子数为9NA | |
| B. | 1mol/L的Mg(NO3)2溶液中含有的NO3-的数目为2 NA | |
| C. | 铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA | |
| D. | 42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2与H2O反应:Cl2+H2O═2H++Cl-+ClO- | |
| B. | Fe与稀硫酸反应:Fe+2H+═Fe3++H2↑ | |
| C. | 氨水与FeCl3溶液反应:3OH-+Fe3+═Fe(OH)3↓ | |
| D. | NaOH与盐酸反应:OH-+H+═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖、硫酸钡和水分别属于非电解质、强电解质、弱电解质 | |
| B. | 甲醇、乙二醇(HOCH2CH2OH)互为同系物 | |
| C. | 除去CO2中混有的SO2:用饱和NaHCO3溶液洗气,再干燥 | |
| D. | 液溴易挥发,盛放在用水密封、玻璃塞塞紧的棕色试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业可采用火法炼铜:Cu2S+O2═2Cu+SO2 每生成2mol铜,反应共转移6NA个电子 | |
| B. | 标准状况下,11.2L甲苯含有的分子数为0.5NA | |
| C. | 20g重水(D2O)所含的电子数为10NA | |
| D. | 60gSiO2中共用电子对数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水显碱性,是因为氨水是一种弱碱 | |
| B. | 氨水和液氨成分相同 | |
| C. | 氨水中物质的量浓度最大的粒子是NH3•H2O(除水外) | |
| D. | 氨水中共有五种粒子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com