
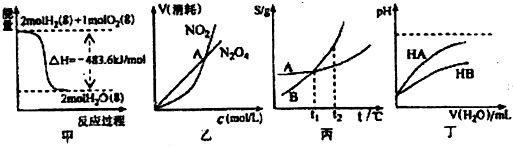
| A�� | �ױ�ʾH2��O2������Ӧ�����е������仯����H2��ȼ����Ϊ483.6kJ•mol-l | |
| B�� | �ұ�ʾ���º��������·����Ŀ��淴Ӧ2NO2?N2O4��g���У������ʵ�Ũ��������������֮��Ĺ�ϵ�����н���A��Ӧ��״̬Ϊ��ѧƽ��״̬ | |
| C�� | ����ʾA��B�����ʵ��ܽ�����¶ȱ仯�������A��B������Һ�ֱ���t1��������t2��ʱ�����ʵ���������B=A | |
| D�� | ����ʾ�����£�ϡ��HA��HB�������ϡ��Һʱ����ҺpH���ˮ���ı仯����ͬŨ�ȵ�NaA��Һ��pH����NaB��Һ |
���� A��ȼ������1mol��ȼ����ȫȼ�������ȶ�������ʱ���ų���������
B������ƽ��ʱ���淴Ӧ������ȣ���Ӧ����֮�ȵ��ڻ�ѧ������֮����������
C�����ݽ�A��B������Һ�ֱ���T1��������T2��ʱ����Һ�����ʺ��ܼ�����������ı�����жϣ�
D��ϡ��HA��HB�������ϡ��Һʱ����ҺpH���ˮ���ı仯��֪����HA����HB���ɴ��ж��ε�ˮ��̶ȣ�
��� �⣺A����101kPaʱ��1mol��ȼ����ȫȼ�������ȶ�������ʱ���ų���������ʹ��ȼ����ʱҪע�������ؼ��㣺�ٷ�Ӧ����������ȼ��Ϊ1mol���ڲ���Ҫ���ȼ�ճ��ȶ��������H��H2O�����������ɵ�ˮΪ���壬����ȼ���ȣ���A����
B���ұ�ʾ���º��������·����Ŀ��淴Ӧ2NO2��g��?N2O4��g���У������ʵ�Ũ��������������֮��Ĺ�ϵ�����������ұ�ʾŨ���������������ϱ�ʾ�����������ʿ죬����ﵽƽ��״̬���������������֮�ȵ��ڻ�ѧ������֮�ȼ�Ӧ�õ���2��1����B����
C����A��B������Һ�ֱ���T1��������T2��ʱ����Һ�����ʺ��ܼ�����������ı䣬������T1���ܽ����ͬ����Ũ����ͬ������T2��ʱ���ʵ�����������ȣ���C��ȷ��
D�������£�ϡ��HA��HB�������ϡ��Һʱ����ҺpH���ˮ���ı仯��֪����HA����HB������NaB��Һ��B?ˮ��̶ȴ�ͬŨ�ȵ�NaA��Һ��pHС��NaB��Һ����D����
��ѡC��
���� ���⿼���Ϊ�ۺϣ��漰ȼ���ȡ���ѧƽ�⡢�ܽ���Լ����ԵıȽϵ����⣬��Ŀ�Ѷ��еȣ������״���ΪB��ע�����ôﵽƽ��״̬ʱ���淴Ӧ���ʵĹ�ϵ�Ƚϣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3COOH��Һ��CH3COOH�ĵ��룺CH3COOH=H ++CH3COO- | |
| B�� | ��CuCl2��Һ������ʵ�飬���ݷ��⣺CuCl2$\frac{\underline{\;���\;}}{\;}$Cu2++2Cl- | |
| C�� | NaHCO3��Һ��HCO3-��ˮ�⣺HCO3-+H2 O?H3 O ++CO32- | |
| D�� | ��FeCl3��Һ����Na2CO3��Һ�У�2Fe3++3 CO32?+3 H2 O�T2Fe��OH��3��+3 CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢۢ� | C�� | �ڢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H=+488.3 kJ•mol-1 | B�� | ��H=-244.15 kJ•mol-1 | ||
| C�� | ��H=-977.6 kJ•mol-1 | D�� | ��H=-488.3 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼��������Һ�еμ�ϡ���� | B�� | ��������Һ�еμ����軯����Һ | ||
| C�� | ��ˮ�еμӵ��۵⻯����Һ | D�� | �Ȼ�����Һ�м��뻹ԭ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������� | B�� | �����ס��� | C�� | ͭ�������� | D�� | п���ӡ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com