
| A. | 某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 | |
| B. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| C. | 25℃时,用pH试纸测定出某醋酸溶液的pH=3.50 | |
| D. | 常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在:K+、Na+、AlO2-、SO42- |
分析 A、溶液pH小于7的溶液有酸、强酸弱碱盐以及强酸的酸式盐等;
B、根据PH大小可计算出溶液中H+浓度,pH=4.5,c(H+)=10-4.5 mol•L-1,pH=6.5,其c(H+)=10-6.5 mol•L-1;
C.NH4Cl溶液中铵根离子水解显酸性;用广泛pH试纸测得PH为整数;
D.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,说明水的电离受到抑制,溶液可能呈酸性,也可能呈碱性;
解答 解:A、某些强酸的酸式盐如NaHSO4溶液的pH<7,故A错误;
B.PH=4.5的番茄汁与pH=6.5的牛奶中c(H+)分别为10-4.5mol•L-1、10-6.5mol•L-1,可见前者c(H+)是后者的100倍,故B正确;
C.25℃时,用pH试纸测定出某醋酸溶液的pH应为整数,故C错误;
D.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,说明水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,如呈碱性,酸溶液中AlO2-离子不能大量共存,故D错误;
故选B.
点评 本题考查了电解质溶液中的有关知识,包括盐类的水解、溶液的pH与c(H+)的关系的判断应用.做题时注意盐溶液类型的积累,对溶液浓度不同类型计算方法的整理以及水的平衡移动的影响条件的理解,题目难度中等.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:推断题
 ,
, ,
,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
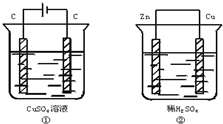 如图两个装置中,溶液体积均为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐水解和溶液体积的变化,则下列叙述正确的是( )
如图两个装置中,溶液体积均为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐水解和溶液体积的变化,则下列叙述正确的是( )| A. | 产生气体的体积:①>② | |
| B. | 电极总质量的变化:①增加,②减小 | |
| C. | 溶液的pH变化:①增大,②减小 | |
| D. | 电极反应式:①装置中的阳极:4OH--4e-→2H2O+O2↑ ②装置中的负极:2H++2e-→H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生石灰、硫、熟石灰 | B. | 液态氧、胆矾、Fe(OH)3胶体 | ||
| C. | 铁、浓硫酸、氯化氮 | D. | 氮气、碘酒、碱式碳酸铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH-CH═CH21,3-二丁烯 | B. | CH2BrCH2Br 二溴乙烷 | ||
| C. | CH3CH2CH(OH)CH33-丁醇 | D. | 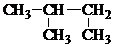 2-甲基丁烷 2-甲基丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8gNa2O2中含有的阴离子数目为0.2Na | |
| B. | 标准状况下,2.24LCHCl3的分子数为0.1NA | |
| C. | 0.1molFe与足量稀HNO3反应,转移电子数为0.3NA | |
| D. | 1L 0.1mol/L Al2(SO4)3溶液中,Al3+的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
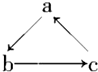 Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是( )
Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是( )| 选项 | A | B | C | D |
| a | Na | Al | Fe | Cu |
| b | NaOH | Al2O3 | FeCl3 | CuSO4 |
| c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com