
【题目】在下图串联装置中,通电片刻即发现乙装置左侧电极表面出现红色固体,则下列说法错误的是

A.当丙中Cu电极质量增加21.6g,甲中共产生4.48 L气体
B.电解过程中丙中溶液pH无变化
C.向甲中加入适量的盐酸,可使溶液恢复到电解前的状态
D.乙中左侧电极反应式:Cu2++2e-=Cu
【答案】AC
【解析】
通电片刻即发现乙装置左侧电极表面出现红色固体,则此红色固体为Cu,即乙装置左侧为阴极,右侧为阳极;甲装置中,左铡电极为阴极,右侧电极为阳极;丙装置中,左侧电极为阴极,右侧电极为阳极。
A. 当丙中Cu电极质量增加21.6g,电路中转移电子0.2mol,甲中产生Cl2 0.1mol,H2 0.1mol,标况下体积为4.48L,因为题中没有强调“标准状况”,所以气体体积不一定是4.48L,A错误;
B. 在丙装置中,阳极Ag-e-=Ag+,阴极Ag++e-=Ag,所以电解过程中丙溶液pH无变化,B正确;
C. 甲中阳极生成Cl2,阴极生成H2,相当于从溶液中逸出HCl气体,若向甲中加入适量的盐酸,则加入了水,溶液浓度减小,不能恢复到电解前的状态,C错误;
D. 乙中左侧铜离子放电,电极反应式:Cu2++2e-=Cu,D正确。
故选AC。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下列说法或表示正确的是( )
A.次氯酸的电离方程式:HClO=H++ClO-
B.只有熵增加的过程才能自发进行
C.HS-水解离子方程式:HS-+H2O![]() H3O++S2-
H3O++S2-
D.已知中和热为57.3 kJ·mol-1,稀硫酸与氢氧化钠稀溶液反应的热化学方程式:H2SO4 (aq)+2NaOH (aq)== Na2SO4 (aq)+2H2O ( l ) ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌-空气电池适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时,下列说法正确的是

A. 电池工作时溶液中的OH-向石墨电极移动
B. Zn电极发生了氧化还原反应
C. 电子经过溶液移向石墨电极
D. 锌电极的电极反应式:Zn + 2OH--2e- = ZnO + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可通过实验来验证淀粉水解生成还原性糖,其实验包括下列一些操作过程,这些操作过程的正确排列顺序是
①取少量淀粉加水制成溶液
②加热煮沸
③加入碱液,中和并呈碱性
④加入新制的Cu(OH)2悬浊液
⑤加入几滴稀H2SO4
⑥再加热
A.①②⑤⑥④③ B.①⑤②③④⑥
C.①⑤②④⑥③ D.①⑥④⑤③②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学——选修3:物质结构与性质)
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是__________________。
(2)A、B、C 三种元素的氢化物稳定性由强到弱的顺序为_________(用化学式表示)。
(3)A的最简单氢化物分子的空间构型为_______,其中A原子的杂化类型是________。
(4)A的单质中δ键的个数为_______________,π键的个数为_______________。
(5)写出基态E原子的价电子排布式:__________________________。
(6)C和D形成的化合物的晶胞结构如图所示,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a =________cm。(用ρ、NA的计算式表示)
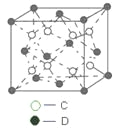
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应![]() 。采取下列措施能加快反应速率的是( )
。采取下列措施能加快反应速率的是( )
①升温 ②恒容下通入惰性气体 ③增加![]() 的浓度 ④减压 ⑤加催化剂 ⑥恒压下通入惰性气体
的浓度 ④减压 ⑤加催化剂 ⑥恒压下通入惰性气体
A.①②⑤B.①③⑤C.②④⑥D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些资料表明:NO、NO2不能与Na2O2反应。某小组学生提出质疑,他们从理论上分析Na2O2和NO2都有氧化性,根据化合价升降原则提出如下假设:
假设Ⅰ. Na2O2氧化NO2; 假设Ⅱ. NO2氧化Na2O2。
请回答下列问题:
(1)甲同学设计如图1所示实验装置:
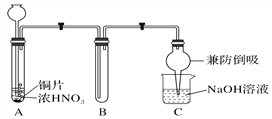
图1
①试管A中反应的离子方程式是___________________________________________________。
②待试管B中收集满气体,向试管B中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。甲同学据此认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的,为达到实验目的,应在A、B之间增加一个装置,该装置的作用是__________________________________________________________________。
③乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失,带火星的木条未复燃。得出结论:假设Ⅰ正确。NO2和Na2O2反应的化学方程式是_____________________。
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化,查阅资料知:
ⅰ) 2NO+Na2O2===2NaNO2;
ⅱ) 6NaNO2+3H2SO4===3Na2SO4+2HNO3+4NO↑+2H2O;
ⅲ)酸性条件下,NO或NO![]() 都能与MnO
都能与MnO![]() 反应生成NO
反应生成NO![]() 和Mn2+。
和Mn2+。
丙同学用图2所示装置(部分夹持装置略)探究NO与Na2O2的反应:
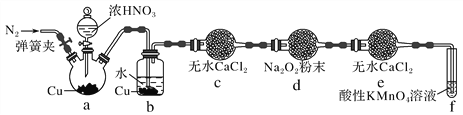
图2
①b装置中观察到的主要现象是__________________________________________________,f装置的作用是_________________________________________________________________。
②在反应前,先打开弹簧夹,通入一段时间N2,其目的是____________________________
③充分反应后,检验d装置中发生反应的实验是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
①氧化剂与还原剂的物质的量比是_______;如果反应生成0.3mol的单质碘,则转移的电子数目是_______。
②先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,这时候,观察到的现象是_____;
③若采用下图实验装置将四氯化碳和I2的混合溶液分离。
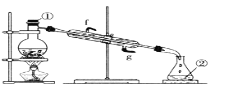
写出图中仪器的名称:①_____;该装置还缺少的仪器是_____;冷凝管的进水口是:_____(填g或f)。
(2)实验室常用MnO2和浓盐酸制氯气,反应原理:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①实验室用MnO2和浓盐酸制氯气的离子方程式:__________________________
②上述反应中氧化剂:__________,还原剂:__________,被氧化的HCl和未被氧化的HCl的比值______________。
③a : Cl2+2I-=I2+2Cl-; b: Cl2+2Fe2+=2Fe3++Cl-; c:2Fe3++2I-=I2+2Fe2+。 Cl2、I2、Fe3+的氧化性由强到弱的顺序:_________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com