
【题目】某化学小组同学在学习Cl2的实验室制法后,发现用加热浓盐酸与MnO2合物的方法制Cl2既浪费能源又不易控制温度,他们现欲对该实验进行改进并验证Cl2的部分性质,进行了如下探究活动。
查阅资料:KMnO4和KClO3的氧化性都比MnO2强,在不加热的条件下均可与浓盐酸发生反应,从而实现制取Cl2的目的。
(1)确定反应原理:![]() __________________
__________________![]()
(2)选择实验装置:现有如图所示的装置,可以选择其中的__________________(填序号)进行实验。

(3)装置的正确连接顺序为__________________(用小写字母序号表示)。
(4)①实验时C中所装液体是__________________。
②在制氯气前,必须进行的一项操作是__________________。
③D中所装液体是__________________。
(5)将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色退去。小组内有甲、乙两种意见。
甲:氯气溶于水后溶液显酸性,中和了NaOH,使溶液退色。
乙:氯气溶于水生成漂白性物质,使溶液退色。
某同学在退色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未显红色,说明_________(填“甲”或“乙”)正确。
【答案】![]() ABCDEGH a→d→e→b(c)→c(b)→g→h→i→j→k→l→f 饱和食盐水 检查装置的气密性 NaOH溶液 乙
ABCDEGH a→d→e→b(c)→c(b)→g→h→i→j→k→l→f 饱和食盐水 检查装置的气密性 NaOH溶液 乙
【解析】
(1)由原子守恒可知,产物中有KCl和MnCl2,配平化学方程式,填入的物质为2KCl+2MnCl2;
(2)KMnO4和浓盐酸反应为固液制备气体的反应,且不需要加热,则反应装置选A,Cl2中含有HCl和H2O,除去HCl,用饱和食盐水溶液洗气,选择装置C,利用装置B干燥,H用于收集氯气,而E和G用于性质验证实验,D用于尾气吸收,综上需要装置包括了ABCDEGH;
(3)装置的正确连接顺序:发生装置→净化装置→性质检验装置→收集装置→尾气处理装置,再净化装置中,先除去HCl,再干燥除水;收集时,由于Cl2的密度大于空气,应该长导管进,则排序为a→d→e→b(c)→c(b)→g→h→i→j→k→l→f;
(4)C的作用是除去挥发出的HC1气体,则C中为饱和食盐水。在制取气体前,应该先检查装置的气密性。吸收多余的Cl2可用NaOH溶液;
(5)因在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液中有酚酞,碱性溶液应显红色,但溶液一直未显红色,说明氯气溶于水生成漂白性物质,使溶液褪色,则乙正确。


科目:高中化学 来源: 题型:
【题目】锡渣主要成分是SnO,还含有少量Fe、Cu、Sb、Pb、As等元素的氧化物.可用下列流程中的方法生产锡酸钠.
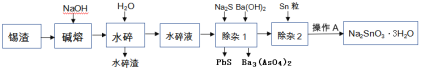
已知: ①砷酸钡难溶于水,Ksp(Ba3(AsO4)2)=10-24
②水碎液中溶质的主要成分为Na2SnO3,Na3AsO4, Na3SbO4,Na2PbO2
(1)碱熔就是在锡渣中加NaOH焙烧,SnO转变为Na2SnO3,则SnO参加反应的化学方程式为____________
(2)除杂1的目的是“除砷和铅”,加入硫化钠所发生反应的离子方程式为____________;若要使0.001mol/L的AsO43-沉淀完全(一般认为离子浓度小于10-6mol/L时即沉淀完全),需等体积加入至少____________mol/L的Ba(OH)2.
(3)除杂2中加入Sn粒的目的是____________
(4)已知Na2SnO3·3H2O可溶于水,难溶于乙醇,加热至140℃时会失去结晶水,所以最后一步从滤液中得到锡酸钠晶体的操作步骤为____________、过滤、用____________洗涤、____________.
(5)水碎渣中的铁元素主要以氧化物形式存在,回收比较容易,而铜冶炼过程中的铜渣中也有铁元素,但主要以硅酸铁的形式存在,回收方法更复杂:需先加CaO作置换剂,发生钙铁置换反应CaO+FeO·SiO2![]() CaO·SiO2+FeO,在反应过程中,加CaO的同时还需加入还原剂烟煤,则加入还原剂烟煤的作用是____________
CaO·SiO2+FeO,在反应过程中,加CaO的同时还需加入还原剂烟煤,则加入还原剂烟煤的作用是____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光.下列有关该电池的说法正确的是( )
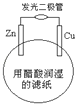
A. 铜片上的电极反应:Cu — 2e﹣ = Cu2+
B. 锌片为电池的负极
C. 外电路中电子由铜片经导线流向锌片
D. 电池工作时电能直接转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
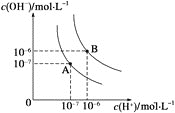
【题目】(1)水的电离平衡曲线如图所示,若A点表示25 ℃时水的电离达平衡时的离子浓度,B点表示100 ℃时水的电离达平衡时的离子浓度。则100 ℃时1 mol·L-1的NaOH溶液中,由水电离出的c(H+)________mol·L-1,Kw(25 ℃)________Kw(100 ℃)(填“>”、“<”或“=”)。25 ℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是________(填“促进”、“抑制”或“不影响”)。
(2)电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为_____________________________。
②25 ℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,则c(Na+)______c(CH3COO-)(填“>”、“<”或“=”)。
③向NaCN溶液中通入少量CO2,所发生反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有Na2SO3、Na2S04混合物样品ag,为了测定其中Na2SO3的质量分数,设计了如下方案,其中明显不合理的是
A. 将样品配制成溶液V1L,取其中25.00 mL用标准KMn04溶液滴定,消耗标准 KMn04 溶液V2 mL
B. 向样品中加足量H202,再加足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为bg
C. 将样品与足量稀盐酸充分反应后,再加入足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为c g
D. 将样品与足量稀盐酸充分反应,生成的气体依次通过盛有饱和NaHS03的洗气瓶、盛有浓H2S04的洗气瓶、盛有碱石灰的干燥管I、盛有碱石灰的干燥管II,测得干燥管I增重dg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“大同”化学小组在实验室中对![]() 进行探究。回答下列问题:
进行探究。回答下列问题:
(1)![]() 学生甲用下图E装置制备
学生甲用下图E装置制备![]() 。主反应的发生,表明硫酸具有的性质有________
。主反应的发生,表明硫酸具有的性质有________

A.氧化性 ![]() 还原性
还原性 ![]() 酸性
酸性 ![]() 碱性
碱性
![]() 学生乙以
学生乙以![]() 粉未和
粉未和![]() 为原料制取
为原料制取![]() ,反应的化学方程式是:___
,反应的化学方程式是:___
![]() 现欲收集一瓶干燥的
现欲收集一瓶干燥的![]() ,选用下图中的A、B、C、D装置,其连接顺序
,选用下图中的A、B、C、D装置,其连接顺序![]() 按气流方向,用小写字母表示,可重复选用
按气流方向,用小写字母表示,可重复选用![]() 为:_________
为:_________
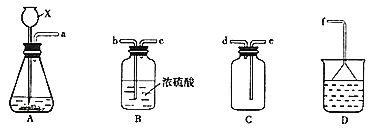
(2)学生丙用浓![]() 和蔗糖反应,得到的气体中含有
和蔗糖反应,得到的气体中含有![]() 、
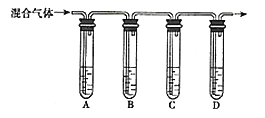
、![]() 。现选择下图中的装置,验证混合气体中存在
。现选择下图中的装置,验证混合气体中存在![]() 和
和![]() 。其中,能证明存在
。其中,能证明存在![]() 的现象是_____。
的现象是_____。
(3)学生甲实验中,大试管内产生了大量黑色固体。查阅资料知:
![]() 黑色固体可能含有CuO、CuS、
黑色固体可能含有CuO、CuS、![]() 。
。
![]() 和
和![]() 不溶于稀盐酸、稀硫酸,但加热下可溶于稀硝酸。
不溶于稀盐酸、稀硫酸,但加热下可溶于稀硝酸。
![]() 向含微量
向含微量 ![]() 的溶液中滴加
的溶液中滴加![]() 溶液,能产生红褐色沉淀。
溶液,能产生红褐色沉淀。
现取少量黑色沉淀,加入稀硫酸,充分振荡以后,再滴加![]() 溶液,未见红褐色沉淀,由此所得结论是_____________________。另取少量黑色沉淀,加入足量稀硝酸并加热,发现黑色固体最终完全溶解,溶液变为蓝色,有无色气泡生成,管口处出现红棕色。试写出CuS溶于足量稀硝酸的离子方程式:__________为测定黑色沉淀中
溶液,未见红褐色沉淀,由此所得结论是_____________________。另取少量黑色沉淀,加入足量稀硝酸并加热,发现黑色固体最终完全溶解,溶液变为蓝色,有无色气泡生成,管口处出现红棕色。试写出CuS溶于足量稀硝酸的离子方程式:__________为测定黑色沉淀中![]() 的百分含量,取
的百分含量,取![]() 黑色沉淀,在酸性溶液中用
黑色沉淀,在酸性溶液中用 ![]() 溶液处理,发生反应如下:
溶液处理,发生反应如下:![]()
![]() ,反应后煮沸溶液,赶尽
,反应后煮沸溶液,赶尽![]() ,过量的高锰酸钾溶液恰好与
,过量的高锰酸钾溶液恰好与![]() 溶液完全反应。则混合物中
溶液完全反应。则混合物中![]() 的质量分数为 ___________
的质量分数为 ___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C2H6(g)![]() C2H4(g)+H2(g) △H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( )
C2H4(g)+H2(g) △H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( )
A. 增大容器容积B. 升高反应温度
C. 分离出部分氢气D. 等容下通入惰性气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定镀锌铁皮锌镀层厚度[ρ(Zn)=7.14gcm-3],某兴趣小组同学截取三块形状规则、大小相近的长方形铁皮(来自同一块镀锌铁皮),量出其长度与宽度,计算得铁片单侧面积;用稀硫酸进行定量试验,数据如下:
实验序号 | 铁片单侧面积/cm2 | 反应前质量/g | 反应后质量/g |
1 | 25.05 | 14.625 | 13.803 |
2 | 24.95 | 14.566 | 13.746 |
3 | 24.89 | 14.489 | 12.789 |
该镀锌铁皮锌镀层厚度为___cm(保留2位有效数字);写出简要计算过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关晶体的叙述不正确的是( )
A.氯化钠和氯化铯晶体中,阴离子的配位数均为6
B.金刚石为空间网状结构,由碳原子以sp3杂化轨道形成共价键
C.金属钠的晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com