
| ʵ�� ��� | ��Ӧ�¶� ������ˮԡ���ȣ� | ϡ���� ��Һ | MnSO4���� | 0.10mol/L KMnO4��Һ | ��ɫ ʱ�� |
| 1 | 65�� | ---- | --- | 1mL | 100s |
| 2 | 65�� | 10�� | --- | 1mL | 90s |
| 3 | 75�� | 10�� | ---- | 1mL | 40s |
| 4 | 75�� | 10�� | �������� | 1mL | 3s |
���� ������ͼ��ʵ�����ݷ������ڶ����Ǽ���ϡ���ᣬ��Ӧ��ɫʱ�����̣������������£���Ӧ���ʽϴ��������������������̷�Ӧ��������������ã�
��1��������Һ���ƺ͵ζ�ʵ�鲽�������Ҫ��������ע����ȡ��Һ������Ǿ�ȷ��ȡ���������ᣬ���������Һ����ǿ�����ԣ���Ҫ����ʽ�ζ��ܣ�
��2��H2C2O4��Һ������KMnO4��Һ��Ӧ����������ԭ��Ӧ���ɶ�����̼�������Ӻ�ˮ��
��3�����ݵζ�ʵ�����ݺ����ӷ���ʽ���㣮
��� �⣺������ͼ��ʵ�����ݷ������ڶ����Ǽ���ϡ���ᣬ��Ӧ��ɫʱ��ȵ�һ�����̣��������������¶ȣ���Ӧ���ʽϴ��������ÿ����10��C��Ӧ��������Ϊԭ����2.25������������������̣���Ӧ������죬Ϊ�������13���࣬˵���������ã�
�ʴ�Ϊ��ϡ�������ʹ������Ӧ���ʼӿ죬���·�Ӧ���ʼӿ����¶�����10��C��Ӧ��������Ϊԭ����2.25����Mn2+���÷�Ӧ�Ĵ������ɼӿ췴Ӧ���ʣ�
��1����������ƽ��ȡ���ᾧ�壨H2C2O4•2H2O��Wg�����Ƴ�250mL��Һ��Ҫ���������������ձ�����ͷ�ιܡ�250mL����ƿ��ÿ����ȡ25.00 mL����Һ����ƿ�У���0.10mol/L���Ը��������Һ�ζ�����Ҫ��ƿ�����������Һ����ǿ�����ԣ�����������ԣ�ѡ����ʽ�ζ���ȷ��ȡ��
�ʴ�Ϊ����ʽ�ζ��ܣ�
��2��H2C2O4��Һ������KMnO4��Һ��Ӧ�����ӷ���Ϊ��5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��++8H2O��
�ʴ�Ϊ��5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��++8H2O��
��3��25ml��Һ�ø��������Һ�ζ������ζ�������ƽ���������Ը��������ҺVmL���������ӷ���ʽ5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��++8H2O������250ml��Һ�в������ʵ���=$\frac{5��V��1{0}^{-3}L��0.10mol/L}{2}$��10=2.5V��10-5mol������ᾧ��Ĵ���Ϊ=$\frac{2.5V��1{0}^{-5}mol��126g/mol}{Wg}$��100%=$\frac{31.5V}{W}%$��
�ʴ�Ϊ��$\frac{31.5V}{W}%$��
���� ���⿼�������ʺ�����ʵ�������ʵ���жϼ��㣬��Һ���ƺ͵ζ�ʵ��ķ���Ӧ�ã�ʵ����ƺ�ʵ����������ջ����ǹؼ�����Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��

| A�� | W��Z��ͬһ���� | |
| B�� | ԭ�Ӱ뾶��W��X��Y��Z | |
| C�� | ��̬�⻯����ȶ��ԣ�Y��X | |
| D�� | W��X�γɵļ�������ֻ���й��ۼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �٢ڢ� | C�� | �ۢ� | D�� | �٢ڢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al3+��Na+��SO42-��Cl- | B�� | Na+��K+��CO32-��SO42- | ||
| C�� | K+��NH4+��Cl-��NO3- | D�� | Na+��Ba2+��Cl-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2SiO3 | B�� | Ca��OH��2 | C�� | Ca��NO3��2 | D�� | Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SiO2 CsCl CBr4 CF4 | B�� | SiO2 CsCl CF4 CBr4 | ||
| C�� | CsCl SiO2 CBr4 CF4 | D�� | CF4CBr4CsCl SiO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
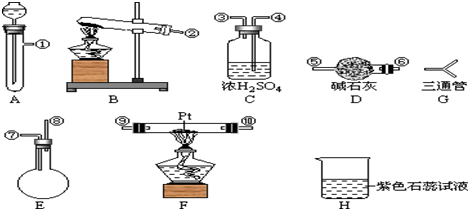
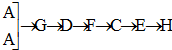 [��װ���Ⱥ�˳������]
[��װ���Ⱥ�˳������]�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͬpH������HX��HY��ǰ�ߵ�Ka��С������ˮϡ�ͺ�pHֵ����ͬ����ǰ������ϡ�͵ı������� | |
| B�� | ��CH3COOH��CH3COONaŨ�Ⱦ�Ϊ0.1mol/L����ϵ�У��������ǿ��ʱ����Һ��PHֵ�����ϴ�仯 | |
| C�� | ��Na2HPO4ˮ��Һ�д��ڹ�ϵʽ��c��H3PO4��+c��H2PO4-��+c��HPO42-��+c��PO43-���Tc��Na+�� | |
| D�� | �����ܽ�ƽ��BaSO4�TBa2++SO42- �ij����ܽ�ƽ�ⳣ��Ϊ1.1��10-10��˵��������BaSO4��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com