
| A、80gNH4NO3 中含有氮原子数为2NA |
| B、1Llmol?L-1盐酸中含有氯化氢分子数为NA |
| C、标准状况下,11.2LCCl4 所含分子数为0.5NA |
| D、铁在氯气中燃烧,1lmolFe失去的电子数为2NA |
| m |
| M |
| 80g |
| 80g/mol |


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
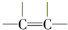 ④-COOH ⑤
④-COOH ⑤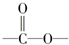 ⑥
⑥
| A、①③④ | B、①③⑤ |
| C、②③④ | D、③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A |
| B |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、92 | B、69 | C、46 | D、32 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 碳纳米管的内部嵌入活泼金属132Cs形成的“包合物”具有很小的密度,有极高的韧性和极强的导电性,有望将来成为优良的导电材料和光电材料.有关这种“包合物”性质的推测合理的是( )
碳纳米管的内部嵌入活泼金属132Cs形成的“包合物”具有很小的密度,有极高的韧性和极强的导电性,有望将来成为优良的导电材料和光电材料.有关这种“包合物”性质的推测合理的是( )| A、具有很强的还原性 |
| B、摩尔质量是144g/mol |
| C、属于原子晶体 |
| D、反应时每摩转移6.02×1023个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、用银氨溶液检验乙醛的醛基:CH3CHO+2Ag(NH3)
| ||||||
B、向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-
| ||||||
| C、向苯酚钠溶液中通入少量的CO2:CO2+H2O+2C6H5O-→ 2C6H5OH+2CO32- | ||||||
| D、甘氨酸(H2N-CH2-COOH)与氢氧化钠溶液反应:H2N-CH2-COOH+OH-→H2N-CH2COO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
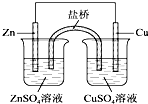
| A、为实现铁上镀铜,可把铁作为阳极 |
| B、氯碱工业通过电解熔融的NaCl生产Cl2 |
| C、如图所示,盐桥中的K+移向ZnSO4溶液 |
| D、氢氧燃料电池(碱性电解质溶液)中O2通入正极,电极反应为O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究性学习小组做了一个如图所示的实验,在导管口点燃氢气后,发现烧杯中酸性溶液褪色,若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色.下列判断正确的是
某研究性学习小组做了一个如图所示的实验,在导管口点燃氢气后,发现烧杯中酸性溶液褪色,若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色.下列判断正确的是| A、该条件下H2燃烧放出的热量使冰分解产生了氧气 |
| B、该条件下H2被冷却为液态氢,液氢的水溶液具有氧化性 |
| C、该条件下生成的物质具有氧化性和还原性 |
| D、该条件下生成的水分子化学性质比较活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH起始读数 | NaOH终点读数 | |
| 第一次 | 0.10mL | 18.60mL |
| 第二次 | 0.30mL | 18.00mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com