
科目:高中化学 来源: 题型:阅读理解

| ||
| ||


 )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸( 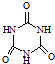 )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过| 化合物 | 密度/g?cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 0.810 | 118.0 | 9 |
| 冰醋酸 | 1.049 | 118.1 | ∞ |
| 乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 通电 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学工业上生产尿素的化学反应是:CO2+2NH3==CO(NH2)2+H2O。已知下列物质在一定条件下均能与水反应产H2和CO2,H2是合成氨的原料,CO2供合成尿素用。若从原料被充分利用的角度考虑,选用_____作原料较好。
A、CO B、石脑油(C5H12、C6H14) C、CH4 D、焦炭
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省龙岩市高三教学质量检测化学试卷 题型:填空题
(12分)Q、W、X、Y、Z是原子序数逐渐增大的短周期元素。已知Q在所有原子中的原子半径最小,W是形成化合物种类最多的元素,Y的最外层电子数是内层电子数的3倍,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物。(注:答题应根据题目要求,用元素符号或化学式来表示对应元素或物质)
(1)Z的离子结构示意图
(2)为了提高工业合成XQ3产率(该反应为放热反应),下列措施合理的是
a.升高温度
b.加入催化剂
c.将XQ3分离出去
d.增大反应体系压强
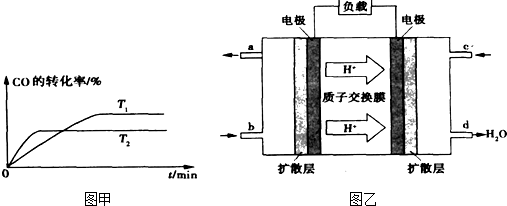
(3)WQ4与Y2反应通过下图装置可将化学能转化为电能。b电极反应式为

(4)标况下2.24LWY2被200mL 1 mol/LZYQ溶液吸收,所得溶液阴离子浓度从大到小的顺序是
(5)下图为某反应体系各物质(均为气体)的量及能量关系,该反应的热化学方程式为 。

(6)X和Z组成的一种离子化合物,能与水反应生成两种碱,其化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年宁夏银川一中高三(上)第三次月考化学试卷(解析版) 题型:解答题
 H2+I2Ⅲ.2H2SO4=2SO2+O2+2H2O
H2+I2Ⅲ.2H2SO4=2SO2+O2+2H2O CH3OH(g)分析该反应并回答下列问题:
CH3OH(g)分析该反应并回答下列问题:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com