
【题目】为解决能源危机,在汽油中掺入一定比例的乙醇(即“乙醇汽油”),以代替一部分汽油。乙醇在气缸中完全燃烧的热化学方程式为:
![]() C2H5OH(l)+
C2H5OH(l)+![]() O2(g)=CO2(g)+
O2(g)=CO2(g)+![]() H2O(l) △H1=-683.4 kJ/mol
H2O(l) △H1=-683.4 kJ/mol
下列说法正确的是
A.该反应过程中,断裂化学键会放出热量
B.该反应中,生成物的总能量大于反应物的总能量
C.乙醇的燃烧热为683.4 kJ/mol
D.反应![]() C2H5OH(l)+
C2H5OH(l)+![]() O2(g)=CO2(g)+
O2(g)=CO2(g)+![]() H2O(g)的△H2>-683.4 kJ/mol
H2O(g)的△H2>-683.4 kJ/mol
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】下列表示水解的离子方程式正确的是( )
A.CH3COO﹣+H2OCH3COOH+OH﹣
B.NH4++H2ONH4OH+H+
C.S2﹣+2H2OH2S+2OH﹣
D.HCO3﹣+H2OH3O++CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种化合物,其中A、C、D焰色反应均为黄色,而B的焰色反应为紫色,A、C和盐酸反应均得到D,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,若B的溶液滴加到硫酸亚铁溶液中,现象为出现白色沉淀→灰绿色沉淀→红褐色沉淀E.试推断:
(1)B:、E:
(2)①C加热分解的化学方程式: ②A与无色无味气体反应的离子方程式:
③由白色沉淀最终变为红褐色沉淀E的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种白色粉末是无水碳酸钠和碳酸氢钠的混合物,称取4.42g灼烧至恒重,把放出的气体通入足量澄清石灰水中,生成2.00g沉淀,灼烧后的残渣能与30mL盐酸恰好完全反应.试求:
(1)该白色粉末灼烧后产生气体在标准状况下的体积?
(2)原混合物中各物质的质量.
(3)所用盐酸的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从第一次学生实验中我们发现,同学们在进行实验时,出现许多不正确的操作方式,希望同学们在今后的实验中,应该克服不规范的操作.请找出下列图示中正确的实验操作( )
A.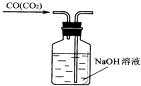
B.
C.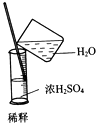
D.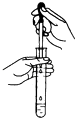
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是“×××”牌饮用矿泉水标签的部分内容. 
请认真阅读标签内容,计算:
(1)镁离子的物质的量浓度的最大值为 .
(2)一瓶合格的这种矿泉水中SO42﹣的物质的量不能超过 . (保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的结构简式为:![]() ,该物质不具有的性质是
,该物质不具有的性质是
A. 与FeCl3溶液发生显色反应 B. 与碳酸氢钠溶液反应生成二氧化碳
C. 与溴水发生取代反应 D. 与乙酸发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W是由A、B两种元素组成的AB2型化合物。
(1)若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛。则W为________(填化学式)。
(2)若取两支试管分别加入少量W溶液,往一支试管中滴入KSCN溶液,无明显现象。往另一支试管中加入足量氯水,再加入适量CCl4,振荡,静置,下层溶液呈紫红色;往上层溶液中滴入KSCN溶液,溶液呈红色。
①W溶液中所含金属阳离子为________。
②上述实验中,W与足量氯水反应的离子方程式为_____________________。
(3)若W是离子化合物,其阴、阳离子均含18个电子,且阴、阳离子个数比为1∶1。
①阴离子的电子式为________。
②1 mol W与足量水充分反应,转移电子的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的CO和CO2相比较,下列叙述中正确的是( )
A.体积比为1:1
B.体积比为11:7
C.原子数比为22:21
D.密度比为11:7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com