
| A. | ①② | B. | ②③ | C. | ①②③ | D. | ①②③④ |
分析 同周期的X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HZO4>H2YO4>H3XO4,则非金属性Z>Y>X,非金属性越强,气态氢化物的稳定性越强,单质的氧化性越强,对应的阴离子的还原性越弱,原子半径逐渐减小,由此分析解答.
解答 解:同周期的X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HZO4>H2YO4>H3XO4,则非金属性Z>Y>X,
①原子的得电子能力为Z>Y>X,原子的得电子能力越强,单质的氧化性越强,对应的阴离子的还原性越弱,故①正确;
②原子的得电子越强,则单质的氧化性越强,原子的得电子能力为Z>Y>X,所以单质的氧化性按X、Y、Z的顺序增强,故②正确;
③同一周期从左到右,元素原子的半径逐渐减小,而原子序数按X、Y、Z的顺序是增大的,所以原子半径按X、Y、Z的顺序减小,故③正确;
④同一周期从左到右,原子的得电子能力越强,气态氢化物的稳定性越强,原子的得电子能力为Z>Y>X,所以稳定性按X、Y、Z的顺序增强,故④错误.
故选C.
点评 本题考查学生同周期内元素性质的递变规律,学生只要知道最高价氧化物对应水化物的酸性越强,中心元素的非金属性越强,然后根据元素性质的变化规律就可以解题了,难度不大.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:解答题
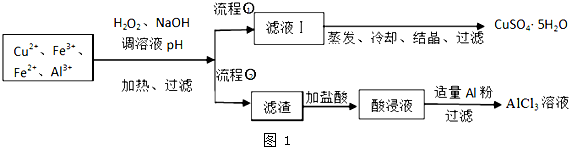
| 离子 | Fe3+ | Fe2+ | Al3+ | Cu2+ |
| pH范围 | 2.2~3.2 | 5.5~9.0 | 4.1~5.0 | 5.3~6.6 |
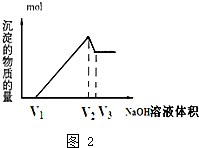
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于元素周期表和元素周期律的发现有突出贡献的科学家是阿伏加德罗 | |
| B. | 元素周期表根据相对原子质量从小到大的顺序排列 | |
| C. | 现常见的元素周期表有七个横行,分为七个周期,有18个纵行,分为16个族 | |
| D. | 每一周期都是从金属元素开始,非金属元素结束 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在量取液体后,量筒中残留的液体要用蒸馏水洗涤并转入相应容器 | |
| B. | 熔融纯碱、烧碱时,不能选用石英坩埚,应该选用铁坩埚 | |
| C. | 蒸发结晶实验中,蒸发皿应放在石棉网上加热 | |
| D. | 在测量或监测温度时,温度计水银球碰到容器内壁不影响测量结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  装置中阳极上析出红色固体 | |
| B. |  装置的待镀铁制品应与电源负极相连 | |
| C. |  装置中粗铜应与电源负极相连 | |
| D. | 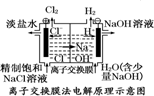 装置的离子交换膜允许阳离子、阴离子、水分子自由通过 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
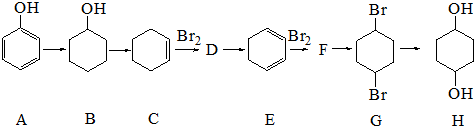
 +2NaOH$\stackrel{醇△}{→}$
+2NaOH$\stackrel{醇△}{→}$ +2NaBr+2H2O.
+2NaBr+2H2O. +Br2→
+Br2→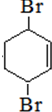 .
. +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 +2H2O.
+2H2O.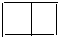 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外电子是分层运动的,像卫星一样有确定的轨道 | |
| B. | 所有电子在同一区域里运动 | |
| C. | 能量高的电子在离核近的区域运动 | |
| D. | 能量低的电子在离核近的区域运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于100mL | B. | 小于100mL | C. | 等于100mL | D. | 等于100/ρ mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com