
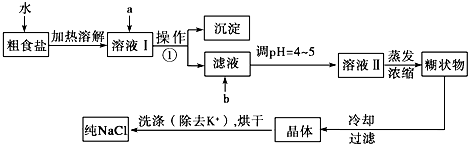
分析 (1)由于过程中加入过量的氯化钡溶液时引入了钡离子,溶液中还有钙离子没出去,故最后加入饱和Na2CO3溶液的目的是在除去溶液中的Ca2+时,同时除去过量的Ba2+;
(2)操作①为过滤,需要用到漏斗、烧杯、玻璃棒;
(3)加入试剂b是为了出去溶液中的氢氧根、碳酸根离子;
(4)洗涤除去NaCl晶体表面附带的少量KCl,用水洗会造成溶质损失,为减少氯化钠晶体的损耗,用75%乙醇溶液洗涤;
(5)检验NaCl晶体中不含有KCl杂质,用焰色反应检验.
解答 解:(1)由于过程中加入过量的氯化钡溶液时引入了钡离子,溶液中还有钙离子没出去,故最后加入饱和Na2CO3溶液的目的是在除去溶液中的Ca2+时,同时除去过量的Ba2+,故答案为:在除去溶液中的Ca2+时,同时除去过量的Ba2+;
(2)操作①为过滤除去不溶性杂质,需要用到漏斗、烧杯、玻璃棒,故答案为:过滤;漏斗、玻璃棒、烧杯;
(3)加入试剂b是为了出去溶液中的氢氧根、碳酸根离子,故需加入稀盐酸,故答案为:稀盐酸;
(4)洗涤除去NaCl晶体表面附带的少量KCl,用水洗会造成溶质损失,为减少氯化钠晶体的损耗,用75%乙醇溶液洗涤,故答案为:75%乙醇溶液;除去氯化钠晶体表面的氯化钾杂质,减少氯化钠晶体的损耗;
(5)检验NaCl晶体中不含有KCl杂质,用焰色反应检验,方法为用洁净的铂丝蘸取少量固体,放置酒精灯火焰灼烧,透过蓝色钴玻璃若无紫色火焰,则证明不含KCl,故答案为:用洁净的铂丝蘸取少量固体,放置酒精灯火焰灼烧,透过蓝色钴玻璃若无紫色火焰,则证明不含KCl.
点评 本题考查海水资源综合应用,为高频考点,涉及流程分析及混合物分离提纯等,把握发生的反应及物质性质为解答的关键,侧重分析与应用能力的考查,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
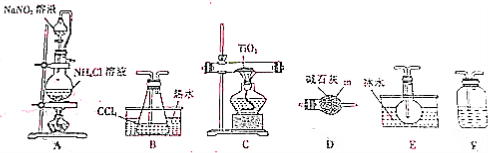
| 物质 | 熔点/℃ | 沸点/℃ | 其它 |
| CCl4 | -23 | 76 | 与 TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾,加热时能被氧气氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
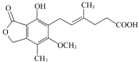
| A. | 该物质的分子式为C17H18O6 | |
| B. | 该物质中含有四种官能团 | |
| C. | 1 mol该物质可与4 mol Br2发生加成反应 | |
| D. | 1 mol该物质与足量金属钠反应产生1 mol氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定量的Na与O2完全反应生成1mol产物时,转移电子数为2NA | |
| B. | 23g乙醇与足量金属钠完全反应时,可生成5.6L氢气 | |
| C. | 1molHCl气体与1molNH3完全反应时,可生成NA个NH4Cl分子 | |
| D. | 若1molCH4与1molCl2光照下充分反应,则生成的一氯甲烷分子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子Cl-、OH-、NO32-、CO32-、X中的一种.
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子Cl-、OH-、NO32-、CO32-、X中的一种.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
元素 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点/℃ | -218,4 | 113 | ? | 450 |
| 单质沸点/℃ | -183 | 444.6 | 685 | 989 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | ? |
| 原子半径/nm | 0.074 | 0.102 | ? | 0.136 |
| 单质与氢化合的难易程度 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com