
����Ŀ����һ��������ܱ������У��������·�Ӧ��CO2��g����H2��g��![]() CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ������ش��������⣺
CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ������ش��������⣺
T/�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��___��
��2���÷�ӦΪ___��Ӧ��ѡ�����ȡ����ȣ���
��3��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c��CO2����c��H2����c��CO����c��H2O�������жϴ�ʱ���¶�Ϊ___�档���¶��¼���2molCO2��g����2molH2��g������ַ�Ӧ���ﵽƽ��ʱ��H2��ת����Ϊ___��
��4����800��ʱ������������Ӧ��ijһʱ�̲�������ڸ����ʵ�Ũ�ȷֱ�Ϊ��CO2��g��Ϊ2 mol/L��H2��g��Ϊ2mol/L��CO��g��Ϊ1mol/L��H2O��g��Ϊ3mol/L���������淴Ӧ���ʵĹ�ϵΪv������___v���棩�����������
���𰸡�c��CO����c��H2O��/c��CO2����c��H2�� �� 830 50�� ��
��������
��1��CO2(g)+H2(g)CO(g)+H2O(g)�Ļ�ѧƽ�ⳣ������ʽK=c(CO)![]() c(H2O)/c(CO2��
c(H2O)/c(CO2��![]() c(H2),��ˣ�������ȷ���ǣ�c(CO)
c(H2),��ˣ�������ȷ���ǣ�c(CO)![]() c(H2O)/c(CO2)
c(H2O)/c(CO2)![]() c(H2);
c(H2);
��2������ͼ����֪�����¶ȵ����ߣ�ƽ�ⳣ��������˵���÷�Ӧ�������ȷ�Ӧ���𰸣�����
ƽ��״̬��ָ���淴Ӧ������ȣ������ʵ������ٸı��״̬����Ը÷�Ӧ��������ϵ����ͬ����Ӧ�����и����ʵ������ʵ����Ƕ�ֵ����ѹǿҲ�Ƕ�ֵ��������Ϊƽ���жϵı�־����d��ֻ��һ�����������Ƿ�ƽ��û�й�ϵ
��3����c(CO2)![]() c(H2)��c(CO)
c(H2)��c(CO)![]() c(H2O)����֪K=1���ɱ������ݿɲ��Ϊ830�棻 ���¶��¼���2molCO2(g)��2molH2(g)����ַ�Ӧ���ﵽƽ��ʱ��
c(H2O)����֪K=1���ɱ������ݿɲ��Ϊ830�棻 ���¶��¼���2molCO2(g)��2molH2(g)����ַ�Ӧ���ﵽƽ��ʱ��
�ɷ�ӦCO2(g) �� H2(g)![]() CO(g)�� H2O
CO(g)�� H2O
��ʼ���� 2/v 2/v 0 0
�仯�� x x x x
ƽ���� 2/v-x 2/v-x x x
K=x2/(2/v-x)2=1�����x=1/v ,H2��ת����=1/2![]() 100
100![]() =50
=50![]() ;
;
�𰸣�830; 50![]() ��
��
��4����ͼ����֪��800��ʱ,K=0.9���ɷ�ӦCO2(g)��H2(g)![]() CO(g)��H2O(g)��֪��Q=1
CO(g)��H2O(g)��֪��Q=1![]() 3/2
3/2![]() 2=0.75<0.9������ƽ��Ӧ�����ƶ���v(��)��v(��0)���𰸣�����
2=0.75<0.9������ƽ��Ӧ�����ƶ���v(��)��v(��0)���𰸣�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��������ʵ�����һ������ȷ����
A. ��FeCl2��Һ�еμ�NH4SCN��Һ����Һ�Ժ�ɫ
B. KAl(SO4) 2��12H2O����ˮ���γ� Al(OH)3����
C. NH4Cl��Ca(OH)2��ϼ��ȿ�����NH3
D. Cu��FeCl3��Һ��Ӧ������CuCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܳ��˵�����淴ӦN2(g)+O2(g)![]() 2NO(g)�Ѵﵽƽ��״̬���ǣ� ��
2NO(g)�Ѵﵽƽ��״̬���ǣ� ��
A. ������ѹǿ����ʱ��ı�
B. �����ڷ�Ӧ�������ʵ�������ʱ��ı�
C. ����������N2��O2��NO�ķ�����֮��Ϊ1:1:2
D. ��λʱ����ÿ����n mo1N2��ͬʱ����2n mo1NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڵ�̼����(K2CO3)Ϊ���Һ����ĭ��Ϊ�缫��������ά��Ϊ��Ĥ��������������ͨ�����ɹ���ֱ��̼ȼ�ϵ�أ���ṹ��ͼ��ʾ������˵����ȷ����
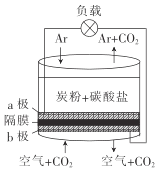
A.�õ�ع���ʱ��CO32-ͨ����Ĥ�ƶ���b��
B.��a������1mol̼�ۣ�ת�Ƶ�����Ϊ4NA
C.b���ĵ缫��ӦʽΪ2CO2+O2-4e-=2CO32-
D.Ϊʹ��س�����������������Ҫ����K2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧʵ��С��Ϊ̽��SO2��Cl2�����ʣ����Ƚ�SO2����ˮ��Ư���ԣ���������µ�ʵ�顣
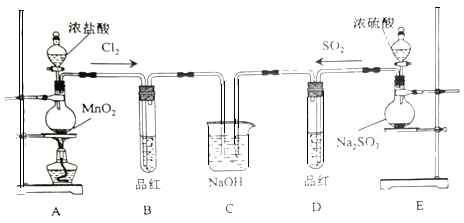
��1��ͼ��ʢ��Ũ��������������Ϊ___��װ��A�з�����Ӧ�Ļ�ѧ����ʽ___��
��2����Ӧһ��ʱ���B��D��Ʒ����ɫ����Ӧ�����ֱ����B��D�е��Թܣ��ɹ۲쵽������Ϊ��B___��D___��
��3��Cװ�õ�����������β����д��SO2������NaOH��Һ��Ӧ�����ӷ���ʽ��___��
��4����ͬѧ��SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һ�У�������ɫЧ���������ԡ����ܵ�ԭ����___���û�ѧ����ʽ��ʾ�������ʵ��֤������ԭ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���2L�ܱ������м���2molN2��10molH2��������ӦN2(g)��3H2(g)![]() 2NH3(g)��2minʱ���ʣ��N2Ϊ1mol�����л�ѧ��Ӧ���ʱ�ʾ����ȷ����(����)
2NH3(g)��2minʱ���ʣ��N2Ϊ1mol�����л�ѧ��Ӧ���ʱ�ʾ����ȷ����(����)
A. v(N2)��0.25 mol��L��1��min��1
B. v(H2)��0.75 mol��L��1��min��1
C. v(NH3)��1 mol��L��1��min��1
D. v(NH3)��0.5 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л��� H���ṹ��ʽΪ 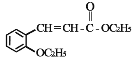 ���Ǻϳɸ߷��ӻ����� M �ĵ��壬H����ͨ���л���A������ʽΪ C7H8O���ͱ�ͪΪԭ�������кϳɣ���ϳ�·�����£�
���Ǻϳɸ߷��ӻ����� M �ĵ��壬H����ͨ���л���A������ʽΪ C7H8O���ͱ�ͪΪԭ�������кϳɣ���ϳ�·�����£�
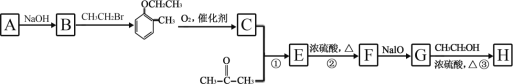
��֪���� ![]()
��
��ش��������⣺
��1��A�ṹ��ʽΪ_____��C �����������ŵ�������_____���ٺ͢۵ķ�Ӧ���ͷֱ���_____��
��2����������������ԭ�Ӽ��鷽��_____��
��3���߷��ӻ�����M �Ľṹ��ʽΪ_____��
��4����Ӧ�۵Ļ�ѧ��Ӧ����ʽΪ_____��
��5���л��� C �ж���ͬ���칹�壬���б�����ֻ�����������ķ�������ͬ���칹����_____�֡�
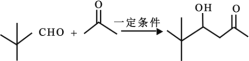
��6������ɱ���ȩ�� 2-�����Ʊ�![]() �ĺϳ�·��_____�����Լ���ѡ����
�ĺϳ�·��_____�����Լ���ѡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ�������ж���ȷ����(����)
A.1mol N2���е�ԭ����ĿΪNA
B.24gMg��ΪMg2+ʱʧȥ�ĵ�����ĿΪ2NA
C.1 molL��1CaCl2��Һ�к��е�Cl����ĿΪ2NA
D.���³�ѹ�£�11.2LCO2�к��е�ԭ����ĿΪ1.5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A. �������һ������1��2�������������һ����ﶼ��4�֣������������칹��
B. CH3CH=CHCH3�����е�����ԭ����ͬһƽ����
C. ��ϵͳ��������������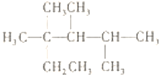 ��������2��3��4-����-2-�һ�����
��������2��3��4-����-2-�һ�����
D. 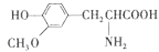 ��
��![]() ����Ϊͬϵ��
����Ϊͬϵ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com