

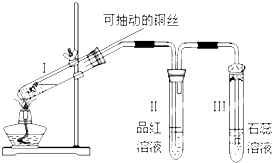
���� ��1��̼��Ũ�����ڼ��������·�Ӧ���ɶ�����̼�����������ˮ���ݴ�д����Ӧ�Ļ�ѧ����ʽ��
��2����Ӧ�ж�����������̼��ˮ�����˱�����ţ�Ӧ��������ˮ����ͭ����ˮ��Ȼ����Ʒ����Һ���ж��������������Ը��������Һ��ȥ����������Ʒ����Һ������������Ѿ�����������ó���ʯ��ˮ���������̼��
��3��E�����ڼ��������̼�ģ�ʢ�ŵ��dz���ʯ��ˮ��
��1�����������ܹ������ⷴӦ���ɵ���S��������������������ԣ�
��2�����Ը��������Һ����ǿ�����ԣ��ܹ��������������������ᣬ���ݻ��ϼ۱仯����������������ʣ�
��3����������Ϊ����������ܹ�������������Һ��Ӧ�����������ͨ����з�̪��NaOH��Һ����Һ��ɫ��
��� �⣺��1��̼��Ũ�����ڼ��������·�Ӧ�ķ���ʽΪ��C+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+2SO2��+2H2O��
�ʴ�Ϊ��C+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+2SO2��+2H2O��
��2��������Һ�к���ˮ��Ҫ���鷴Ӧ��������ȼ���ˮ��ʹ���Լ�Ϊ��ˮCuSO4��ĩ����������Ͷ�����̼���ܹ�ʹ����ʯ��ˮ����ǣ�����Ӧ���ȼ����������Ȼ������������������������̼������D��Ʒ����Һ��ɫ��֤�����������Ѿ�������
�ʴ�Ϊ����ˮCuSO4��ĩ��ˮ��Ʒ�첻��ɫ��
��3��D��Ʒ����Һ����ɫ��֤�����������Ѿ���������D���ڼ��������̼��ʢ�ŵ��dz���ʯ��ˮ���������ʯ��ˮ����ǣ���֤���������ж�����̼��
�ʴ�Ϊ������ʯ��ˮ��CO2��
��1���������������ⷴӦ����S���ʣ�����������S�Ļ��ϼ۴�+4�۽�Ϊ0�ۣ�������������������ԣ�����֤��SO2���������ԣ�Ӧ����C�н��������ᣬ
�ʴ�Ϊ�������
��2������������S�Ļ��ϼ�Ϊ+4�ۣ��ܹ���ǿ���������Ը��������Һ������+6�ۣ���Ӧ�ж�����������˻�ԭ�ԣ�
�ʴ�Ϊ����ԭ��
��3��E�м�����з�̪��NaOH��Һ����Һ����ɫ��֤�����������ܹ�������������Һ��Ӧ�����������Ϊ���������
�ʴ�Ϊ���ᣮ
���� ���⿼����Ũ��������ʡ�������������ʼ����飬��Ŀ�Ѷ��еȣ�ע������Ũ����Ļ�ѧ���ʣ���ȷ��������ʼ�������Ⱥ�˳��Ϊ���ؼ�������������ѧ���ķ�����������ѧʵ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
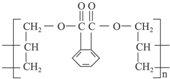 �ϳ����ĵ�������У�������
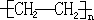
�ϳ����ĵ�������У�������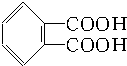 �� �ڱ�ϩ����CH2�TCH-CH2OH��
�� �ڱ�ϩ����CH2�TCH-CH2OH�� | A�� | �٢� | B�� | �ۢ� | C�� | �ܢ� | D�� | �ܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
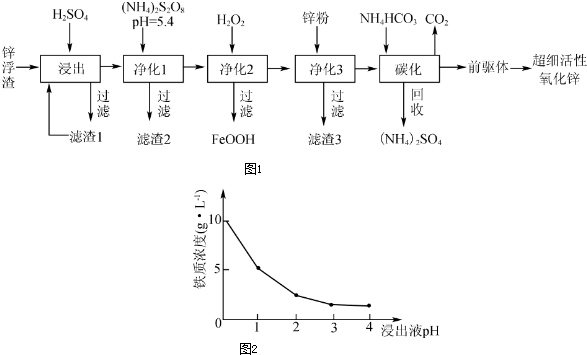
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
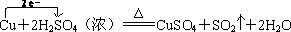 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
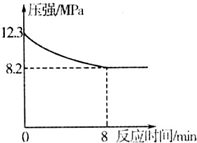
| A�� | ˮ��ȴ��0������ʱ��ɱ�������Ϊˮ���Ӵ�Һ�����˹��� | |
| B�� | �����������¶ȱ仯ʱ���ܱ��ֳ���̬�仯 | |
| C�� | �������¶ȣ�ֻ����ѹǿ��Ҳ����ʹ���ʴ���̬��ɹ�̬ | |
| D�� | ������������������Ϊ�������ʵ����ܹ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
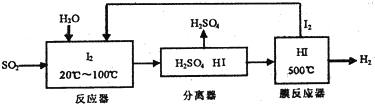
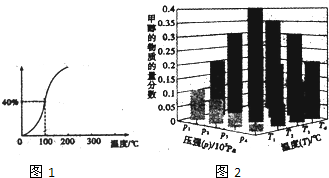
 �о�̼���仯��������ʶ��ڿ��С��������������Ҫ���壮
�о�̼���仯��������ʶ��ڿ��С��������������Ҫ���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ��t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| ��ѹǿp/100kPa | 4.56 | 5.14 | 5.87 | 6.30 | 7.24 | 8.16 | 8.18 | 8.20 | 8.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com