
分析 加热发生反应:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,导致固体质量减少,利用差量法计算原混合物中NaHCO3的质量、生成碳酸钠的质量,利用反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O,根据CO2的质量可计算加热后总的Na2CO3的质量,减去NaHCO3分解生成的Na2CO3的质量即可得原混合物中Na2CO3的质量.
解答 解:加热发生反应方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,导致固体质量减少:4g-3.38g=0.62g,
设混合物中有NaHCO3的质量为x,新生成的Na2CO3的质量为y,
2NaHCO3=Na2CO3+CO2↑+H2O△m
168g 106g 62g
x y 4g-3.38g=0.62g
解得x=$\frac{168g×0.62g}{62g}$=1.68g,y=$\frac{106g×0.62g}{62g}$=1.06g,
所以生成碳酸钠的物质的量为0.01mol,根据碳守恒原混合物中碳酸钠的物质的量为:$\frac{0.448L}{22.4L/mol}$-0.01mol=0.01mol,
答:原混合物中 Na2CO3 的物质的量为 0.01 mol.
点评 本题考查学生化学方程式的有关计算知识,题目难度中等,掌握碳酸钠、碳酸氢钠的化学性质为解答本题的关键,注意差量法在化学计算中的应用方法.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol H3PO4的质量为98g.mol-1 | B. | H3PO4的摩尔质量为98 g | ||
| C. | 9.8 g H3PO4含有NA个H3PO4分子? | D. | NA个H3PO4分子的质量为98g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
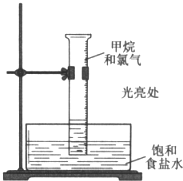 甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )
甲烷与氯气在光照条件下发生反应(装置如图),实验现象及解释均正确的是( )| 现象 | 解释 | |
| A. | 量筒内气体颜色逐渐变浅 | 甲烷被氯气还原 |
| B. | 量筒内出现少量白雾 | 生成HCl气体 |
| C. | 量筒内壁产生油状液滴 | 油状液体是CCl4 |
| D. | 量筒中液面降低 | 生成液态产物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 | 实验结论 |
 | 溶液变为黄色 | 氧化性:Cl2>Br2 |
 | 溶液变为黄色 | 氧化性: Br2>I2 |
 | 溶液的颜色由黄色变为蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 通电时阴极附近溶液的酸性增强 | |
| B. | 铅蓄电池的A极为正极 | |
| C. | 通电时,H+由左至右通过质子交换膜 | |
| D. | 通电时,Pt电极的质量几乎不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1 | B. | 1mol•L-1 | C. | 3mol•L-1 | D. | 1.5mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com