


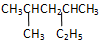 的系统命名是:2,4-二甲基己烷
的系统命名是:2,4-二甲基己烷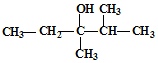 的键线式是
的键线式是
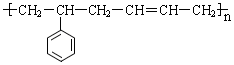 的单体结构简式为:
的单体结构简式为: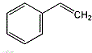 和CH2=CH-CH=CH2
和CH2=CH-CH=CH2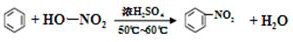

分析 (1)-OH中含一个未成对电子;
(2)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小;
(3)烷烃命名时,选最长的碳链为主链,从离支链近的一端给主链上的碳原子编号;
(4)在有机物的键线式中,拐点和端点代表碳原子,含氧官能团不能省略;
(5)在判断高聚物单体时,如果是多条碳碳单键相连,隔一条断一条;如果有碳碳双键,应考虑单体为二烯烃或炔烃;
(6)苯与浓硫酸、浓硝酸的混合酸在50~60℃时发生取代反应,生成硝基苯;
(7)丙烯分子中含有碳碳双键,在一定条件下能够发生加聚反应生成聚丙烯,据此写出该反应的化学方程式;
(8)2-溴丙烷在氢氧化钠的醇溶液中发生消去反应生成丙烯、溴化钠和水.
解答 解:(1)电子式是用原子的最外层电子表示出来的式子,故羟基的电子式为 ,故答案为:
,故答案为: ;
;
(2)三硝基甲苯中苯环与N原子相连,正确的结构简式为: ,故答案为:
,故答案为: ;
;
(3)烷烃命名时,选最长的碳链为主链,故此有机物的主链上有6个碳原子,称为己烷,从离支链近的一端给主链上的碳原子编号,故在2号和4号碳原子上各有一个甲基,故名称为2,4-二甲基己烷,故答案为:2,4-二甲基己烷;
(4)只用键线来表示碳架,两根单键之间或一根双键和一根单键之间的夹角为120?,一根单键和一根三键之间的夹角为180?,而分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略,而其他杂原子及与杂原子相连的氢原子须保留.用这种方式表示的结构式为键线式; 的键线式为:
的键线式为: ;
;
故答案为: ;
;
(5)在判断高聚物单体时,如果是多条碳碳单键相连,隔一条断一条;如果有碳碳双键,应考虑单体为二烯烃或炔烃,故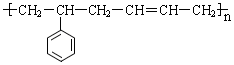 的单体为苯乙烯和1,3-丁二烯,结构简式为
的单体为苯乙烯和1,3-丁二烯,结构简式为 和CH2=CH-CH=CH2,
和CH2=CH-CH=CH2,
故答案为: ;CH2=CH-CH=CH2;
;CH2=CH-CH=CH2;
(6)苯与浓硫酸、浓硝酸的混合酸在50~60℃时发生取代反应,生成硝基苯,反应为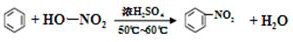 ,
,
故答案为: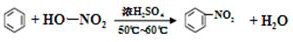 ;
;
(7)聚丙烯分子中含有不饱和的碳碳双键,在一定条件下能够发生加聚反应得到聚丙烯,反应的化学方程式为: ,
,
故答案为: ;
;
(8)2-溴丙烷在氢氧化钠的醇溶液中发生消去反应生成丙烯、溴化钠和水,反应的化学方程式为CH3CHBrCH3+NaOH→CH3-CH=CH2↑+NaBr+H2O,
故答案为:CH3CHBrCH3+NaOH→CH3-CH=CH2↑+NaBr+H2O.
点评 本题考查有机物化学反应方程式的书写,为高频考点,把握常见有机物的性质及反应类型为解答的关键,注意有机反应条件,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 铜制品在潮湿空气中生锈,其主要原因是发生了析氢腐蚀 | |
| B. | 铜的电解精炼工业中,沉积在电解槽底部的阳极泥可作为提炼金、银等贵重金属的原料 | |
| C. | 泡沫灭火器中所装试剂为Na2CO3和Al2(SO4)3 | |
| D. | 从海水中可以制取NaCl,电解饱和NaCl溶液可以制金属Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01 | B. | 100 | C. | 0.1 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铝溶液中加入过量氨水 Al3++3OH-═Al(OH)3↓ | |
| B. | 碳酸钠溶液中加入澄清石灰水 Ca(OH)2+CO32-═CaCO3↓+2OH- | |
| C. | 向NaHCO3溶液中加入少量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 稀硫酸中加入铁粉 2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 成分 | SiO2 | MgO | Fe2O3 | Al2O3 | CuO |
| 质量分数(%) | ? | 4.0 | 32 | 10.2 | 16 |
| Cu(OH)2 | Mg(OH)2 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀的pH | 4.8 | 9.3 | 2.7 | 3.8 |
| 完全沉淀的pH | 6.4 | 10.8 | 3.7 | 4.7 |
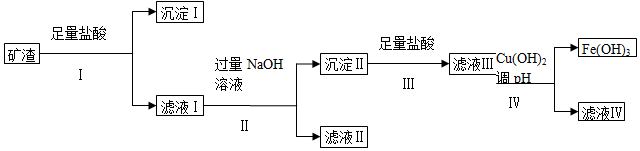
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 3 | C. | 4 | D. | 2 或 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com