
【题目】下列物质中,既有离子键又有共价键的是( )
A.CaCl2
B.KOH
C.H2O
D.HF
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 常温下,10 mL 0.02 mol·L-1 HCl溶液与10 mL 0.02 mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
B. 在0.1 molL﹣1 CH3COONa溶液中:n(OH﹣)+0.1mol>n(CH3COOH)+n(H+)+n(Na+)
C. 在10mL 0.1 mol/L的AgNO3溶液中加入6mL等浓度的NaCl溶液,有白色沉淀产生,再加入6 mL等浓度的Na2S溶液,溶液中又有黑色沉淀生成,说明Ksp(Ag2S)< Ksp(AgCl)
D. 常温下pH=4的NaHC2O4溶液中:c(H2C2O4)>c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃以任意比例混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L。下列各组混合烃中符合此条件的是( )
A. CH4C2H4 B. CH4C3H6 C. C2H6C3H4 D. C2H2C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列装置或操作能达到实验目的的是________(填字母序号,下同)。

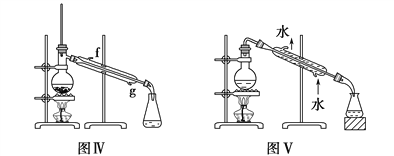
a.除去乙醇中的乙酸用图Ⅰ装置 b.形成原电池用图Ⅱ装置
c.制取乙酸乙酯用图Ⅲ装置 d.石油的蒸馏用图Ⅳ装置
e.分离Na2CO3溶液和CH3COOC2H5用图Ⅴ装置
(2)“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
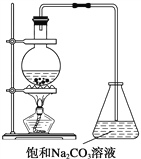
(1)写出制取乙酸乙酯的化学反应方程式____________。
(2)浓硫酸的作用是:
①_____________; ②_____________。
(3)做此实验时,还需向盛乙酸和乙醇的装置里加入几块碎瓷片,其目的是:____________________________。
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是: __________________________________。
(5)用方程式表示为什么不能用NaOH溶液代替饱和Na2CO3溶液的原因:______。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是___________。
(7)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)_____________________。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在自来水蒸馏实验中,下列操作不正确的是( )
A. 在蒸馏烧瓶中盛约1/3体积的自来水,并放入几粒沸石
B. 可以不用温度计
C. 冷水从冷凝管上口入,下口出
D. 取少量收集到的液体滴入硝酸银和稀硝酸,无明显现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂排放的废水中可能含有K+、Ag+、NH4+、Mg2+、SO42-、Cl-、NO3-、HCO3-等离子。经检测废水呈明显的碱性,则可确定该厂废水中肯定不含有的离子组合是( )
A. Ag+、K+、NO3-、HCO3- B. Ag+、NH4+、Mg2+、HCO3-
C. K+、NH4+、NO3-、SO42- D. K+、Mg2+、SO42-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子方程式BaCO3+2H+===CO2↑+H2O+Ba2+中的H+不能代表的物质( )
①H2SO4 ②NaHSO4 ③HNO3 ④HCl ⑤CH3COOH
A.①②⑤ B.①④⑤ C.②④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、N、M元素,它们在周期表中位罝如图所示,下列说法不正确的是
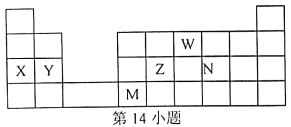
A. 离子半径:W>X>Y B. 单质的还原性:X>Y>N
C. 硒与元素N同主族,最高价氧化物的水化物的酸性比N的弱 D. 元素M位于金属与非金属的分界线附近,推测M元素的单质一定可以做半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com