
| A、用氨水鉴别Al3+、Mg2+和Ag+ |
| B、用Ba(NO3)2溶液鉴别Cl-、SO42-和CO32- |
| C、用水鉴别乙醇、甲苯、硝基苯 |
| D、用KMnO4酸性溶液鉴别苯、甲苯、环己烷 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、①⑤⑥ | B、②③④⑤ |
| C、①③④ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.8mol/L |
| B、1 mol/L |
| C、1.6 mol/L |
| D、1.9mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7834Se和8034Se互为同位素 |
| B、7834Se和8034Se都含有34个中子 |
| C、7834Se和8034Se分别含有44和46个质子 |
| D、7834Se和8034Se含有不同的电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
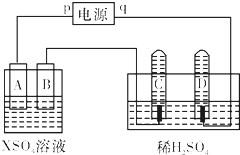 如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡.试回答:
如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡.试回答:| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极生成气体体积 (cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极生成气体体积 (cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定有Mg |
| B、若有Al则一定有Fe |
| C、若有Cu则一定有Al |
| D、若有Mg则一定有Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
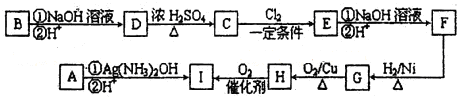
查看答案和解析>>
科目:高中化学 来源: 题型:
| 条件改变 | 结论 | |
| A | 平衡后向容器中充入1molHe | 平衡常数不变,混合气体的密度也不变 |
| B | 起始时向容器中充入0.5molSO2、0.25molO2和2molSO3 | 反应达到平衡前v(正)>v(逆) |
| C | 起始时向容器中充入1molSO2和0.5mol O2 | 达到平衡时共放出78.4kJ的热量 |
| D | 起始时向容器中充入1molSO2和0.5molO2 | 达到平衡时,SO2的转化率为60% |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com