
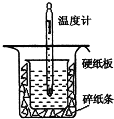
 �к��ȵIJⶨ�Ǹ�����Ҫ�Ķ���ʵ�飮ȡ0.55mol/L��NaOH��Һ50mL��0.50mol/L������50mL������ͼ��ʾ��װ���н����к��ȵIJⶨʵ�飬�ش��������⣺
�к��ȵIJⶨ�Ǹ�����Ҫ�Ķ���ʵ�飮ȡ0.55mol/L��NaOH��Һ50mL��0.50mol/L������50mL������ͼ��ʾ��װ���н����к��ȵIJⶨʵ�飬�ش��������⣺| ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | �²t2-t1���� | ||
| ���� | NaOH��Һ | ƽ��ֵ | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
| 2 | 25.1 | 25.1 | 25.1 | 28.5 | 3.4 |
| 3 | 25.1 | 25.1 | 25.1 | 28.6 | 3.5 |
���� ��1���������ȼƵĹ������жϸ�װ�õ�ȱ��������Ϊ�˼�����������ʧ�����ձ�������С�ձ�������ƽ��
��2�����ݻ��Һ������ж��ձ��Ĺ��
��3�����ж��¶Ȳ����Ч�ԣ�Ȼ������¶Ȳ�ƽ��ֵ��Ȼ�����Q=m•c•��T���㷴Ӧ�ų���������Ȼ����ݡ�H=-$\frac{Q}{n}$kJ/mol�������Ӧ�ȣ�
��� �⣺��1�������ȼƵĹ����֪��װ�õ�ȱ�������ǻ��β����������Ϊ�˼�����������ʧ�����ձ�������С�ձ�������ƽ��ͼʾװ����С�ձ���δ��Ӳֽ���ס������ձ�����ֽ�������ˣ�δ��С�ձ�����㹻�ߣ���
�ʴ�Ϊ�����β����������С�ձ���δ��Ӳֽ���ס������ձ�����ֽ�������ˣ�δ��С�ձ�����㹻�ߣ���
��2������������Һ��������Һ�������Ϊ100mL����С�ձ��Ĺ��Ӧ��Ϊ100mL��
�ʴ�Ϊ���ڣ�
��3��3���¶Ȳ�ֱ�Ϊ��3.3�棬3.4�棬3.5�棬���ݾ���Ч���¶Ȳ�ƽ��ֵΪ3.4�棬0.55mol/L��NaOH��Һ50mL��0.50mol/L������50mL�����кͷ�Ӧ����ˮ�����ʵ���Ϊ0.05L��0.50mol=0.025mol����Һ������Ϊ��100ml��1g/ml=100g���¶ȱ仯��ֵ��TΪ3.4�������㣬������0.025molˮ�ų�������ΪQ=m•c•��T=100g��4.18J/��g•�棩��3.4��=1421.2J����1.421kJ������ʵ���õ��к��ȡ�H=-$\frac{1.421kJ}{0.025mol}$=-56.8 kJ/mol��
�ʴ�Ϊ��-56.8 kJ/mol��
���� ���⿼�����к��ȵIJⶨ����Ŀ�Ѷ��еȣ�ע�������к��ȵĸ���ⶨ��Ӧ�ȵķ�������ȷ�к��ȵļ��㷽��������������ѧ���Ļ�ѧ����ͻ�ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ʊ������������壺����ڵ�NaOH��Һ�У��μ��Ȼ���������Һ����������ɫ | |
| B�� | �ᴿ���������ӵı�����������������Һ�����÷�Һ������ȥ�л����ˮ | |
| C�� | �������������Ƿ���ʣ��������ܽ������Ȼ�����Һ���۲�ʵ������ | |
| D�� | �Ƚ�����ͭ�Ļ����ԣ���ͭ�ۼ���1.0��mol•L-1��Fe2��SO4��3��Һ�У��۲�ʵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
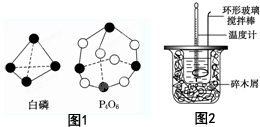
 Na2CO3��NaHCO3�����ᷴӦ��ЧӦ�IJⶨ������ͼ��ʾ���Ӻ�װ�ã�Ϊ̽��NaHCO3��Na2CO3�����ᷴӦ�����е���ЧӦ������ʵ�鲢����������ݣ�
Na2CO3��NaHCO3�����ᷴӦ��ЧӦ�IJⶨ������ͼ��ʾ���Ӻ�װ�ã�Ϊ̽��NaHCO3��Na2CO3�����ᷴӦ�����е���ЧӦ������ʵ�鲢����������ݣ�| ��� | 48mL�Լ� | ���� | ���ǰ�¶�/�� | ��Ϻ��¶�/�� |
| �� | ˮ | 2 g NaHCO3 | 20.0 | 18.6 |
| �� | ˮ | 2 g Na2CO3 | 20.0 | 21.6 |
| �� | ���ᣨ0.1mol•L-1�� | 2 g NaHCO3 | 20.0 | 17.2 |
| �� | ���ᣨ0.1mol•L-1�� | 2 g Na2CO3 | 20.0 | 22.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
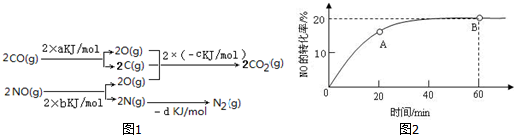
 ��1����֪��2SO2��g��+O2�T2SO3��g����H=-196.6kJ•mol-1��2NO��g��+O2�T2NO2��g����H=-113.0kJ•mol-1����ӦNO2��g��+SO2��g���TSO3��g��+NO��g�� �ġ�H=-41.8kJ/mol��
��1����֪��2SO2��g��+O2�T2SO3��g����H=-196.6kJ•mol-1��2NO��g��+O2�T2NO2��g����H=-113.0kJ•mol-1����ӦNO2��g��+SO2��g���TSO3��g��+NO��g�� �ġ�H=-41.8kJ/mol���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl2��Fe3+��Cu2+��MnO2 | B�� | MnO2��Cl2��Fe3+��Cu2+ | ||
| C�� | Fe3+��Cu2+��MnO2��Cl2 | D�� | Cu2+��Fe3+��Cl2��MnO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
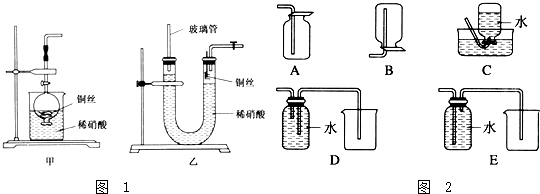
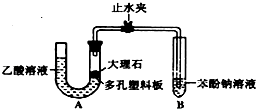 ijУѧ��С��Ϊ̽�����ᡢ̼��ͱ��ӵ�����ǿ����֤������Ϊ���ᣬ��������ʵ�飮
ijУѧ��С��Ϊ̽�����ᡢ̼��ͱ��ӵ�����ǿ����֤������Ϊ���ᣬ��������ʵ�飮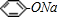 ��Һ
��Һ�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com