
【题目】工业上电解 Na2CO3的原理如图所示。下列说法不正确的是( )

A. 阴极产生的物质 A 是 H2
B. 电解一段时间后,阳极附近溶液的 PH 将增大
C. 该离子交换膜应为阳离子交换膜
D. 阳极电极反应为 4CO32-+2H2O-4e-=4HCO3-+O2↑
【答案】B
【解析】
工业上电解 Na2CO3溶液,根据装置图分析,电解池阳极发生的反应为物质失去电子,发生氧化反应,碳酸钠转化为碳酸氢钠,则阳极电极反应为:4CO32-+2H2O-4e-=4HCO3-+O2↑,阴极为物质得到电子,发生还原反应,生成氢氧化钠,则阴极反应式为:2H2O+2e-═2OH-+H2↑,据此分析判断。
A. 阴极发生还原反应,反应式为:2H2O+2e-═2OH-+H2↑,则阴极产生的物质A是H2,故A正确;
B. 阳极电极反应为:4CO32-+2H2O-4e-=4HCO3-+O2↑,溶液的碱性减弱,所以电解一段时间后,阳极附近溶液的 pH 将减小,故B错误;
C. 由于阴极产品为氢氧化钠,阳极区的钠离子要进入阴极区,所以离子交换膜应为阳离子交换膜,故C正确;
D. 阳极发生氧化反应,阳极电极反应为 4CO32-+2H2O-4e-=4HCO3-+O2↑,故D正确。
故选B。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】欲测定含少量氯化钠的小苏打固态样品中NaHCO3的质量分数可用以下四种方法。
方法一:
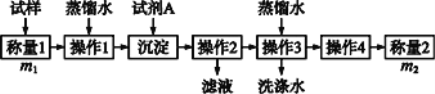
方法二:
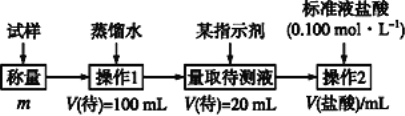
方法三:
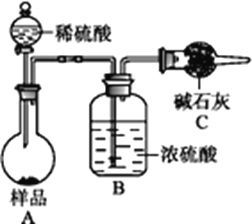
方法四:不使用化学试剂,使用实验室常用仪器。
按要求回答下列问题:
(1)方法一:加入足量的试剂A是___________(填写A的化学式),可将HCO3-转化为沉淀并称重。操作1、2、3、4的名称依次是溶解、____、洗涤和干燥(烘干);
(2)方法二:在操作1中所用到的玻璃仪器中,除了烧杯、玻璃棒、胶头滴管外,还需要用到的是__________,应选择甲基橙作指示剂;
(3)在方法二中计算该样品中NaHCO3的质量分数为_____________;
(4)在方法三中,根据所用的实验装置,除了称量样品质量外,还需测定的实验数据是_____________________;
(5)仔细分析方法三中的实验装置,若由此测得的数据来计算实验结果,则有可能偏高也有可能偏低,偏高的原因可能是_________,偏低的原因可能是__________(均文字简述);
(6)方法四的实验原理是________________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用16mol/L 浓硫酸配制100mL 2.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容 ⑥摇匀。回答下列问题:
(1)该实验所需的玻璃仪器:______、玻璃棒、烧杯、胶头滴管、量筒。
(2)所需浓硫酸的体积是_____,量取浓硫酸所用的量筒的规格是____(规格从下列中选用A.10mL B.20mL C.50mL D.100mL)。
(3)第⑤步定容的具体实验操作是_______。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.容量瓶用蒸馏水洗涤后残留有少量的水____。
B.转移溶液前未冷却至室温_____。
C.定容时仰视溶液的凹液面______。
D. 向容量瓶中转移溶液时,不慎有少量溶液洒在容量瓶外面____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图在衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴含有酚酞的澄清石灰水、FeCl2溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿。提示:实验室中所用的少量氯气可以用下述原理制取:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应在常温下即能进行。
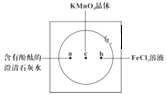
(1)浓盐酸在反应中表现出来的性质是______ (填写编号),氧化剂与还原剂物质的量之比为______ ,氧化产物为______ 。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(2)产生0.1 mol Cl2,则转移电子的物质的量为 ______ mol。
(3)a处反应的化学方程式是___________________________,工业上用此原理制取漂白粉。
(4)b处离子方程式是________________________。
(5)高锰酸钾标准溶液经常用来滴定测量物质的含量。用高锰酸钾法间接测定石灰石中CaCO3的含量的方法为:称取试样0.1250g,用稀盐酸溶解后加入(NH4)2C2O4得CaC2O4沉淀。沉淀经过滤洗涤后溶于稀硫酸中。滴定生成的H2C2O4用去浓度为0.016mo/LKMnO4溶液25.00mL。
①写出CaC2O4沉淀溶解的离子方程式:___________________
②配平并完成下列高锰酸钾滴定草酸反应的离子方程式: ____MnO4-+___H2C2O4+____=___Mn2++___CO2↑+____
③石灰石中CaCO3的百分含量:_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,相同温度下,在容器Ⅰ和Ⅱ中分别充入等物质的量的HI,发生反应2HI(g) ![]() H2(g)+I2(g)。下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法不正确的是( )
H2(g)+I2(g)。下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法不正确的是( )
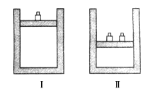
A. Ⅰ和Ⅱ中活化分子数相同
B. Ⅰ和Ⅱ中活化分子百分数相同
C. Ⅰ和Ⅱ中单位体积内活化分子数相等
D. Ⅰ中化学反应速率比Ⅱ中的小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于难溶电解质溶解平衡的说法正确的是
A. 可直接根据 Ksp 的数值大小比较难溶电解质在水中的溶解度大小
B. 在 AgCl 的饱和溶液中,加入蒸馏水, Ksp(AgCl)不变
C. 难溶电解质的溶解平衡过程是可逆的,且在平衡状态时 v溶解=v沉淀=0
D. 25℃时, Ksp(AgCl)>Ksp(AgI),向 AgCl 的饱和溶液中加入少量 KI 固体,一定有黄色沉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁(![]() )广泛应用于航天、化工等领域中,其电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂),下列说法正确的是( )
)广泛应用于航天、化工等领域中,其电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂),下列说法正确的是( )
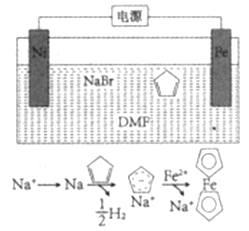
A. 该电解池的阳极反应Fe-3e-=Fe3+
B. DMF溶液可用水替代
C. 电解液中钠离子起到催化剂的作用
D. 该过程中消耗2mol环戊二烯理论上产生22.4L的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色实验均为黄色。
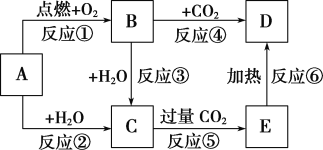
(1)写出下列物质的化学式:B________;E___________。
(2)以上6个反应中属于氧化还原反应的有________(填写编号)。
(3)写出B→C反应的离子方程式:________________________________________;
C→E的化学方程式:____________________________________________;
E→D的化学方程式:___________________________________________;
(4)加热5.00 g D和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31 g,则原混合物中D的质量为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com