
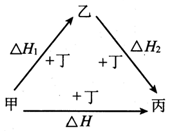
 甲、乙、丙、丁四种物质在一 定条件下的转化关系如图所示,当乙作为反应物且与甲的物质的量相等时,△H=△H1+△H2.则甲、丙可能是( )
甲、乙、丙、丁四种物质在一 定条件下的转化关系如图所示,当乙作为反应物且与甲的物质的量相等时,△H=△H1+△H2.则甲、丙可能是( )| A. | S、SO3 | B. | AlCl3、NaAlO2 | C. | Na、Na2O2 | D. | NaOH、Na2CO3 |
分析 A.硫与氧气反应,只能一步生成二氧化硫;
B.甲、丙分别为AlCl3、NaAlO2,丁为NaOH,乙为Al(OH)3,且符合转化中的能量变化;
C.甲、丙分别为Na、Na2O2,乙为Na2O,丁为O2,但从方程式可知,乙作为反应物且与甲的物质的量相等时,不能满足△H=△H1+△H2;
D.甲为NaOH,丙为Na2CO3,碳酸氢钠与二氧化碳不能反应生成碳酸钠.
解答 解:A.因S与氧气反应生成二氧化硫,不会直接生成三氧化硫,则甲不能转化为丙三氧化硫,不符合转化,故A错误;
B.由AlCl3+4NaOH═3NaCl+NaAlO2+2H2O,可看成AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O来完成,甲为AlCl3,丙为NaAlO2,丁为NaOH,乙为Al(OH)3,且Al(OH)3与AlCl3的物质的量相等,符合△H=△H1+△H2,故B正确;
C.由2Na+O2,$\frac{\underline{\;点燃\;}}{\;}$Na2O2,可看成2Na+$\frac{1}{2}$O2═Na2O、Na2O+$\frac{1}{2}$O2═Na2O2来完成,甲为Na、乙为Na2O,丙为Na2O2,丁为O2,乙、甲的物质的量相等时,不符合△H=△H1+△H2,故C错误;
D.甲为NaOH,丙为Na2CO3,由2NaOH+CO2═Na2CO3+H2O可看成NaOH+CO2═NaHCO3,但碳酸氢钠与二氧化碳不能反应生成碳酸钠,不符合转化,故D错误;
故选B.
点评 本题考查元素化合物知识以及反应中△H的关系,明确一步完成的反应可由哪些反应分步来完成及物质的物质的量的关系是解答本题的关键,题目难度中等.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 离子组 | X试剂 | 离子方程式 |
| A | K+、Na+、ClO-、SO42- | 少量SO2 | SO2+ClO-+H2O═SO42-+Cl-+2H+ |
| B | NH4+、Fe3+、Br-、SO42- | 过量H2S | 2Fe3++H2S═2Fe2++S↓+2H+ |
| C | NH4+、Na+、Fe3+、[Al(OH)4]- | 过量铜粉 | 2Fe3++Cu═2Fe2++Cu2+ |
| D | K+、Na+、HCO3-、Al3+ | 少量HCl | H++HCO3-═CO2↑+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
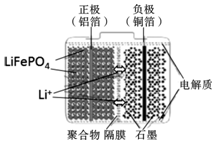 磷酸铁锂电池装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐.电池工作时的总反应为:LiFePO4+6C$?_{放电}^{充电}$ Li1-xFePO4+LixC6,则下列说法正确的是( )
磷酸铁锂电池装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐.电池工作时的总反应为:LiFePO4+6C$?_{放电}^{充电}$ Li1-xFePO4+LixC6,则下列说法正确的是( )| A. | 图中聚合物隔膜是阴离子交换膜 | |
| B. | 充电时,Li+迁移方向是“由右向左” | |
| C. | 放电时,正极的电极反应式为LiFePO4-xe-=Li1-xFePO4+xLi+ | |
| D. | 用该电池电解精炼铜,当转移电子1.25mol时能得到精铜32g,则电子利用率为80% |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 |
| ①取少量固体于试管中,加入足量蒸馏水 | 得到无色溶液和白色不溶物 |
| ②向上述试管中加入足量稀盐酸 | 有气泡冒出,白色不溶物部分溶解 |
| ③将步骤②所得物过滤,取部分滤液于试管中,向其中加入少量硝酸银溶液 | 有白色沉淀生成 |
| ④另取步骤③所得滤液少许于试管中,向其中加入足量氢氧化钠溶液 | 无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2 054 | 1 535 | 1 462 |
| 沸点/℃ | 2 467 | 2 980 | 2 750 | - |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
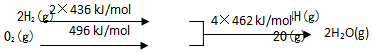
| A. | C(s)的燃烧热110 kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H1=+480 kJ/mol | |
| C. | C(s)+H2O(g)═CO(g)+H2(g)△H1=+130 kJ/mol | |
| D. | 欲分解2 mol H2O(l),至少需要提供4×462 kJ 的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ | ||||
| 四 | ⑪ | ⑫ | ⑬ | |||||

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯是化学物质,不可用作水果的催熟剂 | |
| B. | 煤经过气化和液化等物理变化可转化为清洁燃料 | |
| C. | 石油是混合物,经分馏后得到汽油、煤油和柴油等纯净物 | |
| D. | 汽油与水互不相溶,但不可以用裂化汽油萃取溴水中的溴 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com