
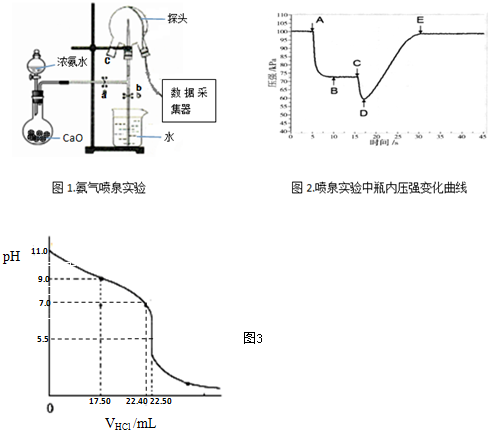
分析 Ⅰ.(1)CaO和水反应生成氢氧化钙且放出热量,放出的热量促进一水合氨分解,据此书写方程式;
氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而导致氨水溶液呈碱性,红色石蕊试液遇碱蓝色,氨气也能和HCl反应生成白烟;
(2)三颈瓶内气体与外界大气压压强之差越大,其喷泉越剧烈;
Ⅱ.(3)可以用移液管或碱式滴定管量取碱性溶液;
(4)根据图知,当氨水和稀盐酸恰好完全反应时混合溶液的pH值为3.5,此时存在c(HCl)×V(HCl)=c(NH3)×V(NH3);
弱电解质电离平衡常数Kb=$\frac{c(O{H}^{-}).c(N{{H}_{4}}^{+})}{c(N{H}_{3}.{H}_{2}O)}$;pH=11的氨水中c(OH-)=0.001mol/L,c(OH-)≈c(NH4+)=0.001mol/L,c(NH3•H2O)≈0.0450mol/L,根据Kb=$\frac{c(O{H}^{-}).c(N{{H}_{4}}^{+})}{c(N{H}_{3}.{H}_{2}O)}$计算电离平衡常数;
(5)A.锥形瓶中有少量蒸馏水不影响氨水的物质的量;
B.利用pH计判断滴定终点更准确;
C.酸式滴定管未用盐酸润洗会导致盐酸浓度偏低;
D.滴定终点时俯视读数会导致盐酸物质的量偏小.
解答 9解:Ⅰ.(1)CaO和水反应生成氢氧化钙且放出热量,放出的热量促进一水合氨分解,该反应方程式为NH3•H2O+CaO=Ca(OH)2+NH3↑;
氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而导致氨水溶液呈碱性,红色石蕊试液遇碱蓝色,氨气也能和HCl反应生成白烟,所以氨气的检验方法为:将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明NH3已收满;或:将蘸有浓盐酸的玻璃棒靠近瓶口c,有白烟生成,证明NH3已收满;
故答案为:NH3•H2O+CaO=Ca(OH)2+NH3↑;
将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明NH3已收满;或:将蘸有浓盐酸的玻璃棒靠近瓶口c,有白烟生成,证明NH3已收满;
(2)三颈瓶内气体与外界大气压压强之差越大,其反应速率越快,D点压强最小、大气压不变,所以大气压和D点压强差最大,则喷泉越剧烈,故答案为:D;
Ⅱ.(3)氨水中含有一水合氨,一水合氨电离出氢氧根离子而使溶液呈碱性,所以用移液管或碱式滴定管量取氨水,故答案为:碱式滴定管(或移液管);
(4)根据图知,当氨水和稀盐酸恰好完全反应时混合溶液的pH值为3.5,此时存在c(HCl)×V(HCl)=c(NH3)×V(NH3),0.0500mol/L×0.0225L=c(NH3)×0.025L,c(NH3)=0.045mol/L;
弱电解质电离平衡常数Kb=$\frac{c(O{H}^{-}).c(N{{H}_{4}}^{+})}{c(N{H}_{3}.{H}_{2}O)}$;pH=11的氨水中c(OH-)=0.001mol/L,c(OH-)≈c(NH4+)=0.001mol/L,c(NH3•H2O)≈0.0450mol/L,根据Kb=$\frac{c(O{H}^{-}).c(N{{H}_{4}}^{+})}{c(N{H}_{3}.{H}_{2}O)}$=$\frac{0.001×0.001}{0.045}$=2.2×10-5;
故答案为:0.045;$\frac{c(O{H}^{-}).c(N{{H}_{4}}^{+})}{c(N{H}_{3}.{H}_{2}O)}$;2.2×10-5;
(5)A.锥形瓶中有少量蒸馏水不影响氨水的物质的量,所以不影响测定结果,故A正确;
B.利用pH计判断滴定终点更准确,不需要酸碱指示剂即可,故B错误;
C.酸式滴定管未用盐酸润洗会导致盐酸浓度偏低,则使用盐酸的体积偏大,所以导致测定结果偏高,故C正确;
D.滴定终点时俯视读数会导致盐酸体积偏小,则盐酸物质的量偏小,测定结果偏低,故D错误.
故选AC.
点评 本题考查性质实验方案设计,侧重考查学生分析、判断及实验操作能力,明确滴定原理、喷泉实验原理、弱电解质电离等知识点是解本题关键,(5)题A为易错点,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 26Fe的价层电子排布式为3d64s2 | |
| B. | 35Br的电子排布式可简写为[Ar]4s24p5 | |
| C. | NH4Cl的电子式为 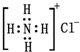 | |
| D. | 氯离子结构示意图为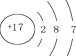 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为a kJ•mol-1 | B. | a一定大于0 | ||
| C. | a+b=-638.5 | D. | b一定小于0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+、Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | ||
| M |
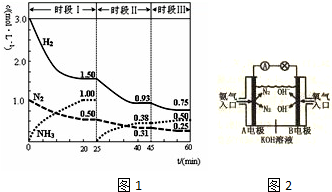
 N2+2CO2,该反应的平衡常数表达式为K=$\frac{c(C{O}_{2})•c({N}_{2})}{{c}^{2}(CO)•{c}^{2}(NO)}$;
N2+2CO2,该反应的平衡常数表达式为K=$\frac{c(C{O}_{2})•c({N}_{2})}{{c}^{2}(CO)•{c}^{2}(NO)}$;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:r(Y2-)>r(Z2+) | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | Y的气态简单氢化物的热稳定性比氮元素的气态简单氢化物弱 | |
| D. | X、Y、Z、W所有元素的最高正价等于其所在族的族序数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
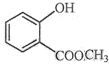 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.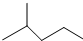 表示的分子式为C6H14;2-甲基-2-丁烯的结构简式为CH3C (CH3)=CHCH3.
表示的分子式为C6H14;2-甲基-2-丁烯的结构简式为CH3C (CH3)=CHCH3. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com