
分析 氢原子物质的量为水的2倍,氧原子物质的量等于水的物质的量,根据N=nNA计算水分子数目;
根据n=$\frac{N}{{N}_{A}}$计算水分子数目,结合氧原子数目相等计算二氧化碳的物质的量.
解答 解:2mol H2O中含H原子为2mol×2=4mol,含有O原子为2mol×1=2mol,H2O分子数目为2mol×6.02×1023mol-1=1.204×1024;
1.806×1024个H2O分子的物质的量为$\frac{1.806×1{0}^{24}}{6.02×1{0}^{23}mo{l}^{-1}}$=3mol,含有的氧原子数相同的 CO2的物质的量为$\frac{3mol}{2}$=1.5mol,
故答案为:4;1;1.204×1024;1.5.
点评 本题考查物质的量有关计算,比较基础,注意对化学式意义的理解,有利于基础知识的巩固.


 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol/L | B. | 0.25 mol/L | C. | 0.1 mol/L | D. | 1 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 状态 | 物质 | 密度 | 1mol该物质的质量 | 1mol该物质的体积 | 结论 |
| 固态 | Fe | 7.86g•cm-3(20℃) | 55.96g | 7.12 cm3 | |
| Al | 2.70g•cm-3(20℃) | 27g | 10.00cm3 | ||
| 液体 | H2O | 0.998g•cm-3(20℃) | 18g | 18.04cm3 | |
| H2SO4 | 1.83g•cm-3(20℃) | 98.00g | 53.55cm3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
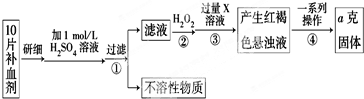
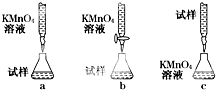
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
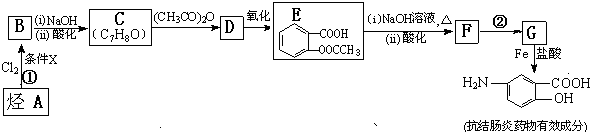
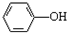 $\stackrel{(CH_{3}CO)_{2}O}{→}$
$\stackrel{(CH_{3}CO)_{2}O}{→}$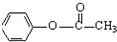
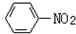 $→_{盐酸}^{Fe}$
$→_{盐酸}^{Fe}$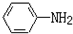
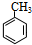 .
. .
. .
.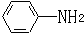 易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此写出以A为原料合成化合物
易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此写出以A为原料合成化合物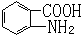 的合成路线
的合成路线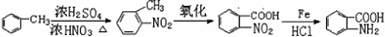 .(仿照题中抗结肠炎药物有效成分的合成路线的表达方式答题)
.(仿照题中抗结肠炎药物有效成分的合成路线的表达方式答题)查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,W与R以1:3的原子个数比形成的化合物的电子式
,W与R以1:3的原子个数比形成的化合物的电子式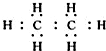 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com