
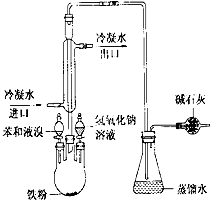
 如图是实验室制取溴苯的装置图
如图是实验室制取溴苯的装置图分析 (1)苯与溴在铁做催化剂条件下发生取代反应生成溴苯和溴化氢;
(2)生成物中有HBr,与水蒸气结合形成白雾;
(3)溴化氢易溶于水,容易发生倒吸,可以用水吸收溴化氢,溴离子与银离子反应生成溴化银;
(4)依据冷凝管的作用以及产物有毒回答;
(5)向三颈烧瓶中加入NaOH溶液,与剩余的溴反应生成NaBr、NaBrO与水,防止污染.
解答 解:(1)苯与溴在铁做催化剂条件下发生取代反应生成溴苯和溴化氢,方程式:C6H6+Br2$\stackrel{Fe}{→}$C6H5Br+HBr;
故答案为:C6H6+Br2$\stackrel{Fe}{→}$C6H5Br+HBr;
(2)生成物中有HBr,与水蒸气结合形成白雾,
故答案为:有白雾生成;
(3)溴化氢易溶于水,容易发生倒吸,所以导管口不能插入锥形瓶中的液面之下,锥形瓶中蒸馏水的作用吸收溴化氢,
故答案为:防止倒吸;吸收溴化氢;Ag++Br-=AgBr↓;
(4)溴与苯发生取代反应生成溴苯与溴化氢,反应放热溴化氢蒸出,与锥形瓶中的水蒸气结合成白雾,故冷凝管的作用是冷凝回流;反应后的尾气中含有HBr和挥发出的Br2,直接排放会污染大气,碱石灰作用是吸收HBr与Br2,防止污染空气;
故答案为:冷凝回流;吸收HBr与Br2,防止污染空气;
(5)反应结束后,向三颈烧瓶中加入NaOH溶液,与剩余的溴反应,除去杂质;
故答案为:除去溴苯中Br2等杂质.
点评 本题考查溴苯的实验室制备,对装置的理解、实验操作等,难度中等,熟悉反应原理及各种物质的化学性质是解题关键.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,16gO3含有NA个氧原子 | |
| B. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| C. | 1mol•L-1MgCl2溶液中含有2NA个Cl- | |
| D. | 1molNa被完全氧化生成Na2O2,失去2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
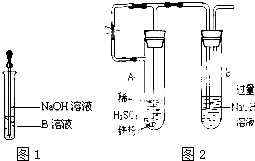 某同学利用右图所示装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质.
某同学利用右图所示装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不管什么反应使用催化剂,都可以加快反应速率 | |
| B. | 可逆反应A(g)?B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大 | |
| C. | 对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大 | |
| D. | 参加反应的物质的性质是决定化学反应速率的主要因素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com