
【题目】现有以下混合液体: ①汽油和氯化钠溶液 ②乙醇与水 ③氯化钠溶液和单质溴,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液
科目:高中化学 来源: 题型:
【题目】欲将氯化钠、沙子(主要成分为SiO2)、碘三种物质组成的固体混合物分离,最科学的操作顺序是
A. 溶解、过滤、加热(升华)、蒸发(结晶)B加热(升华)、 溶解、过滤、蒸发(结晶) B. 升华、溶解、蒸馏、结晶
C. 溶解、结晶、过滤、升华
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SiO2广泛存在于自然界中,其在工业生产中有着广泛的用途。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)==6CaO(s)+P4(s)+10CO(g) ΔH1=+3 359.26 kJ·mol-1
CaO(s)+SiO2(s)==CaSiO3(s) ΔH2=-89.61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)==6CaSiO3(s)+P4(s)+10CO(g) ΔH3 则ΔH3=________ kJ·mol-1。
(2)工业上用石英砂和焦炭可制得粗硅。
已知:
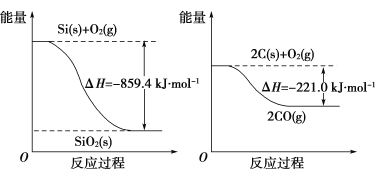
请将以下反应的热化学方程式补充完整:
SiO2(s)+2C(s)==Si(s)+2CO(g) ΔH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对物质的分类正确的是( )
A. SO2、NH3属于电解质
B. 海水、氢氧化铁胶体属于纯净物
C. H2SO4、HNO3属于化合物
D. 烧碱、纯碱属于碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探讨浓度对化学平衡的影响,某同学对可逆反应 “2Fe3++2I-![]() 2Fe2++I2 △H<0”按下图所示步骤进行了一系列实验。
2Fe2++I2 △H<0”按下图所示步骤进行了一系列实验。

说明:0.005 mol·L-1的Fe2(SO4)3溶液颜色接近于无色。
(1)实验中要待实验Ⅰ溶液颜色不再改变时,才能进行实验Ⅱ,目的是 。
(2)实验Ⅱ中,ⅰ的现象是 ,该实验证明 。
(3)实验Ⅱ中,ⅲ的化学平衡向 移动(填“正反应方向”或“逆反应方向”);ⅲ的现象是溶液变浅,该现象 (填“能”或“不能”)说明化学平衡发生移动。如果前一空填“能”,则下一空不填;如果前一空填“不能”,则ⅲ的目的是 。
(4)实验Ⅱ中,ⅱ的现象是 ,即能证明增大生成物浓度化学平衡发生了逆向移动。
(5)除了上图中的方法外,若要使该可逆反应的化学平衡逆向移动,还可以采用的方法有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.为减少碳排放,科学家提出利用CO2和H2反应合成甲醇,其反应原理为CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
(1)上述反应常用CuO和ZnO的混合物作催化剂。经研究发现,催化剂中CuO的质量分数对CO2的转化率和CH3OH的产率有明显影响。实验数据如表所示:

根据数据表判断,催化剂中CuO的最佳质量分数为________。
(2)已知:①CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH1=-41 kJ·mol-1;
CO2(g)+H2(g) ΔH1=-41 kJ·mol-1;
②CO(g)+2H2(g)===CH3OH(g) ΔH2=-91 kJ·mol-1。
写出由CO2和H2制备甲醇蒸气并产生水蒸气的热化学方程式:______________________________。
(3)甲醇是清洁能源。某甲醇燃料电池的电解质为稀硫酸,其能量密度为5.93 kW·h·kg-1。该电池的负极反应式为______________。若甲醇的燃烧热为ΔH=-726.5 kJ·mol-1,该电池的能量利用率为________(结果精确到小数点后1位数字)。(已知1 kW·h=3.6×106 J)
Ⅱ.利用CO和H2在催化剂的作用下合成甲醇,发生如下反应:CO(g)+2H2(g) ![]() CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1 mol CO和2 mol H2,向乙中加入2 mol CO和4 mol H2,测得不同温度下CO的平衡转化率如图2所示。
CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1 mol CO和2 mol H2,向乙中加入2 mol CO和4 mol H2,测得不同温度下CO的平衡转化率如图2所示。
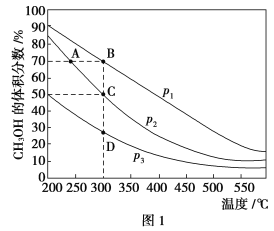
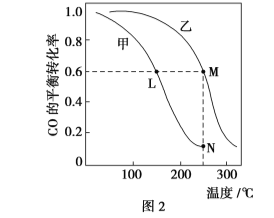
(1)该反应的ΔH________(填“>”、“<”或“=”,后同)0,p1________p2。
(2)达到平衡时,反应速率:A点________B点。平衡常数:C点________D点。
(3)在C点时,CO的转化率为________。
(4)L、M两点容器内压强:p(M)________2p(L)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸生产中,500 ℃时,NH3和O2可能发生如下反应:
①4NH3 (g)+5O2(g) ![]() 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
ΔH=-9 072 kJ·mol-1 K=1.1×1026
②4NH3(g)+4O2(g) ![]() 2N2O(g)+6H2O(g)
2N2O(g)+6H2O(g)
ΔH=-1104.9 kJ·mol-1 K=4.4×1028
③4NH3(g)+3O2(g) ![]() 2N2 (g)+6H2O(g)
2N2 (g)+6H2O(g)
ΔH=-1 269.02 kJ·mol-1 K=7.1×1034
其中,②、③是副反应。若要减少副反应,提高单位时间内NO的产率,最合理的措施是( )
A.增大O2浓度
B.使用合适的催化剂
C.减小压强
D.降低温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中物质的量最多的是(NA表示阿伏伽德罗常数)
A. 1 mol CO2
B. 标准状况下44.8 L H2
C. 3NA个水分子
D. 1 L 1 mol/L的碳酸钠溶液中含的溶质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用中和滴定法测定某烧碱的纯度,实验过程如下:
(1)配制待测液:称取4.100 g固体烧碱样品(杂质不与酸反应)配制成250 mL溶液。
(2)滴定:①用 量取10.00 mL待测液。②向锥形瓶中加入几滴酚酞,用0.2000 mol·L-1的标准盐酸滴定待测烧碱溶液,边滴边摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,直到 时停止滴定。
(3)数据处理
实验次序编号 | 盐酸溶液体积V/mL | 氢氧化钠溶液体积V/mL |
1 | 19.90 | 10.00 |
2 | 20.10 | 10.00 |
3 | 22.00 | 10.00 |
4 | 20.00 | 10.00 |
根据上述表格,选取合适的数据,计算所配待测溶液的物质的量浓度 ,烧碱的纯度为 (保留两位小数)。
(4)一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。某研究性学习小组在实验室中配制盐酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是 (多选)
A.实验中所用到的滴定管、容量瓶,在使用前均需要检漏
B.如果实验中需用80 mL的稀盐酸标准溶液,配制时应选用100 mL容量瓶
C.容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小
D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀盐酸,则测得的NaOH溶液的浓度将偏大
E.配制标准溶液时,定容时俯视读数,则导致实验结果偏大
F.中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大
G.锥形瓶用蒸馏水洗浄后,有少量蒸馏水残留,则导致实验结果偏小
H.滴定前滴定管尖嘴有气泡,滴定后气泡消失,则导致实验结果偏大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com