
·ÖĪö £Ø1£©Ģś·ŪÓŠŹ£Óą£¬øł¾ŻĄė×ÓŃõ»ÆŠŌFe3+£¾Cu2+£¾Fe2+£¬·“Ó¦µÄ·“Ó¦·½³ĢŹ½ĪŖ£ŗ2FeCl3+FeØT3FeCl2”¢CuCl2+FeØTCu+FeCl2£¬ČÜŅŗÖŠŅ»¶Ø“ęŌŚŃĒĢśĄė×Ó£¬ŌŁøł¾Ż·½³ĢŹ½½ųŠŠĻą¹Ų¼ĘĖć£»
£Ø2£©ĪŽ¹ĢĢå³Į»żĪļ“ęŌŚ£¬ĖµĆ÷Ģś·Ū²»×ć£¬ČÜŅŗÖŠµÄĶĄė×Óƻӊ²ĪÓė·“Ó¦£®
½ā“š ½ā£ŗ£Ø1£©ÓÉÓŚĢś·ŪÓŠŹ£Óą£¬ĒŅŃõ»ÆŠŌFe3+£¾Cu2+£¾Fe2+£¬ĖłŅŌČÜŅŗÖŠCu2+ŗĶFe3+ĶźČ«ÓėĢś·Ū·“Ó¦£¬·“Ó¦µÄ·“Ó¦·½³ĢŹ½ĪŖ£ŗ2FeCl3+FeØT3FeCl2”¢CuCl2+FeØTCu+FeCl2£¬·“Ó¦ŗóČÜŅŗÖŠÖ»“ęŌŚFe2+£¬Ć»ÓŠFe3+”¢Cu2+£¬øł¾ŻĀČĄė×ÓŹŲŗć£ŗn£ØCl-£©=£Ø1mol/L”Į3+1mol/L”Į2+1mol/L”Į2£©”Į0.1L=0.7mol£¬ĖłŅŌn£ØFe2+£©=$\frac{1}{2}$n£ØCl-£©=0.35mol£»øł¾Ż·½³ĢŹ½£»2FeCl3+FeØT3FeCl2”¢CuCl2+FeØTCu+FeCl2£¬·“Ó¦ĻūŗÄĢśµÄĮæĪŖn£ØFe£©=$\frac{1}{2}$n£ØFeCl3£©+n£ØCu£©=$\frac{1}{2}$”Į1mol/L”Į0.1L+1mol/L”Į0.1L=0.15mol£¬ÖŹĮæĪŖ£ŗ0.15mol”Į56g/mol=8.4g£¬·“Ӧɜ³ÉµÄĶĪŖn£ØCu£©=1mol/L”Į0.1L=0.1mol£¬ÖŹĮæĪŖ£»0.1mol”Į64g/mol=6.4g£¬¹ĢĢåÖŹĮæ¼õÉŁ8.4g-6.4g=2g£»
¹Ź“š°øĪŖ£ŗ¢ŁFe2+£»0.35mol£»¢ŚCu”¢Fe£»ÉŁ£»2£»
£Ø2£©·“Ó¦Ķź±Ļŗó£¬ĪŽ¹ĢĢå³Į»żĪļ“ęŌŚ£¬ĖµĆ÷ČÜŅŗÖŠµÄĶĄė×Óƻӊ²Ī¼Ó·“Ó¦£¬ĢśĄė×ÓæÉÄÜĒ”ŗĆ·“Ó¦£¬ÓŠæÉÄÜÓŠŹ£Óą£¬·“Ó¦ŗóµÄČÜŅŗÖŠŅ»¶Ø“ęŌŚFe2+”¢Cu2+£»
²»¹ÜĢśĄė×ÓŹĒ·ńÓŠŹ£Óą£¬ĶĄė×ÓµÄĪļÖŹµÄĮæĪŖ¶ØÖµ£¬ĪļÖŹµÄĮæ=1mol/L”Į0.1L=0.1mol£»
¹Ź“š°øĪŖ£ŗFe2+”¢Cu2+£»Cu2+£»0.1mol£®
µćĘĄ ±¾Ģāæ¼²éFeÓėFe3+”¢Cu2+µÄ·“Ó¦£¬ÄѶČÖŠµČ£®ŅŖ×¢Ņāøł¾Ż¹ĢĢåµÄ³É·ÖĮĖ½ā·“Ó¦µÄĻČŗóĖ³Šņ£¬“Ó¶ųČ·¶ØČÜŅŗµÄ³É·Ö£®


 æ¼Ē°±ŲĮ·ĻµĮŠ“š°ø
æ¼Ē°±ŲĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĀČ»ÆĢśČÜŅŗøÆŹ“Ķ°å£ŗCu+Fe3+ØTCu2++Fe2+ | |
| B£® | Óưדה¢µķ·Ūµā»Æ¼ŲŹŌÖ½¼ģŃé¼ÓµāŃĪŹĒ·ńŗ¬µā£ŗ5I-+IO3-+6H+=3I2+3H2O | |
| C£® | ĻņCa£ØHCO3£©2ČÜŅŗÖŠ¼ÓČė¹żĮæµÄNaOHČÜŅŗ£ŗCa2++HCO3-+OH-=CaCO3”ż+H2O | |
| D£® | ÓĆ½ą²Ž¼Į£ØÖ÷ŅŖ³É·ÖHCl£©Óė“óĄķŹÆ·“Ó¦£ŗCaCO3+2H+=Ca2++CO2”ü+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅØĮņĖį | B£® | Ļ”ŃĪĖį | C£® | “×Ėį | D£® | ÅØĻõĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | a mol | B£® | £Øa+0.1£©mol | C£® | 0.05 mol | D£® | ĪŽ·Ø¼ĘĖć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬²āµĆ“×ĖįÄĘČÜŅŗµÄpH£¾7 | |
| B£® | “×ĖįæÉŅŌŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±äŗģ | |
| C£® | ĪļÖŹµÄĮæÅضČĻąĶ¬Ź±£¬ŠæĮ£øśŃĪĖį·“Ó¦µÄĖŁĀŹ±ČÓė“×Ėį·“Ó¦µÄæģ | |
| D£® | ³£ĪĀĻĀ£¬²āµĆ0.1 mol/L“×ĖįČÜŅŗµÄpH£¾1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚæÕĘųÖŠŗÜĪČ¶Ø | B£® | ŃęÉ«·“Ó¦ĻŌ»ĘÉ« | ||
| C£® | ÓėĖ®·“Ó¦·Å³öĒāĘų | D£® | °ė¾¶±ČÄĘŌ×ÓŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 29£ŗ8£ŗ13 | B£® | 22£ŗ1£ŗ14 | C£® | 13£ŗ8£ŗ29 | D£® | 26£ŗ16£ŗ57 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŖĖŲŠŌÖŹµÄÖÜĘŚŠŌ±ä»ÆŹĒŌŖĖŲ»ÆŗĻ¼Ū³ŹÖÜĘŚŠŌ±ä»ÆµÄ±ŲČ»½į¹ū | |
| B£® | ŌŖĖŲÖÜĘŚ±ķÖŠ£¬Ō×ÓµÄ×īĶā²ćµē×ÓŹż¶¼µČÓŚøĆ×åŌŖĖŲµÄ×åŠņŹż | |
| C£® | µŚČżÖÜĘŚÖŠ£¬Ėę×ÅŗĖµēŗÉŹżµÄŌö¼Ó£¬ŌŖĖŲµÄĄė×Ó°ė¾¶Öš½„¼õŠ” | |
| D£® | Ėę×ÅŗĖµēŗÉŹżµÄŌö¼Ó£¬VIIA ×åŌŖĖŲµ„ÖŹµÄČŪ”¢·ŠµćÖš½„Éżøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
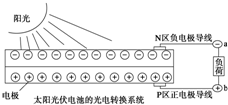
| A£® | ¹ā·ü·¢µēŹĒ½«Ģ«ŃōÄÜ×Ŗ±äĪŖµēÄÜ | |
| B£® | GaÓėNŌŚŌŖĖŲÖÜĘŚ±ķÖŠ²»“¦ÓŚĶ¬Ņ»Ö÷×å | |
| C£® | YAGÖŠīĘĻŌ+3¼Ū | |
| D£® | ÉĻĶ¼ÖŠNĒų°ėµ¼ĢåĪŖøŗ¼«£¬PĒų°ėµ¼ĢåĪŖÕż¼«£¬µēĮ÷“ÓaĮ÷Ļņb |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com