
| A. | Kb(NH3•H2O) | B. | n(OH-) | C. | $\frac{{c({N{H_3}•{H_2}O})}}{{c({O{H^-}})}}$ | D. | $\frac{{c({O{H^-}})}}{{c({NH_4^+})}}$ |
分析 将浓度为0.1mol/L的氨水加水不断稀释,一水合氨的电离程度逐渐增大,则溶液中铵根离子、氢氧根离子的物质的量增大,一水合氨的物质的量减小,同一溶液中,则$\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$的比值逐渐减小;温度不变,一水合氨的电离平衡常数、水的离子积不变,由于稀释过程中氢氧根离子浓度减小,则氢离子浓度增大,据此进行判断.
解答 解:A.稀释过程中温度不变,则一水合氨的电离平衡常数不变,故A错误;
B.稀释过程中一水合氨的电离程度增大,则溶液中氢氧根离子的物质的量增大,故B错误;
C.稀释过程中氢氧根离子的物质的量增大,一水合氨的物质的量减小,同一溶液中,则$\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$的比值逐渐减小,故C正确;
D.稀释过程中一水合氨电离出来的氢氧根离子和铵根离子浓度同比例减小,水的电离使氢氧根离子浓度减小幅度小于铵根离子,故D错误;
故选C.
点评 本题考查了弱电解质的电离平衡及其影响,题目难度中等,明确影响电离平衡的因素为解答关键,易错选项为D,注意稀释过程中水的电离的影响,试题培养了学生的灵活应用能力.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
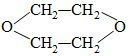
| A. | 乙烯 | B. | 1-丁稀 | C. | 1,3-丁二烯 | D. | 乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、OH-、Cl- | B. | Cu2+、Cl-、SO42-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ca2+、HCO3-、NO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (4)(5)(8) | B. | (1)(4)(5)(7)(8) | C. | (4)(5)(7)(8) | D. | (2)(3)(4)(5)(8) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9.2mol/L | B. | 大于9.2mol/L | C. | 小于9.2mol/L | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 药物阿司匹林可由水杨酸制得,它们的结构如图所示,有关说法正确的( )
药物阿司匹林可由水杨酸制得,它们的结构如图所示,有关说法正确的( )| A. | 服用阿司匹林,身体出现水杨酸不良反应时,可静脉注射NaHCO3溶液 | |
| B. | 阿司匹林的分子式为C9H10O4 | |
| C. | 1mol阿司匹林最多可消耗2molNaOH | |
| D. | 水杨酸可以发生取代,加成,氧化,加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com