
| A、c (CH3COO-)<c (Na+) |
| B、c (CH3COOH)+c (CH3COO-)=0.01mol/L |
| C、c (CH3COOH)>c (CH3COO-) |
| D、c (OH-)>c (H+) |


科目:高中化学 来源: 题型:
| A、漂白精的有效成分是NaClO |
| B、碘化钾的水溶液遇淀粉现蓝色 |
| C、硫在空气中燃烧生成SO2,在纯氧中生成SO3 |
| D、漂白精露置空气中变质,既发生氧化反应又发生非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 熔融盐燃料电池具有高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池正极电极反应式为:O2+2CO2+4e-═2CO32-.试回答下列问题:
熔融盐燃料电池具有高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池正极电极反应式为:O2+2CO2+4e-═2CO32-.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验要求 | 化学试剂 | 供选择的化学试剂 |
| 验证味精中是否含有食盐 | A.新制氢氧化铜悬浊液 B.硝酸银和硝酸 C.碘水 D.碳酸钠粉末 | |
| 证明地瓜粉中含有淀粉 | ||
| 检验食醋中含有乙酸 | ||
| 区别蔗糖和葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:
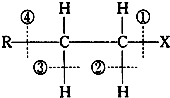
| A、当卤代烃发生水解反应时,被破坏的键是①和④ |
| B、当卤代烃发生水解反应时,被破坏的键是① |
| C、当卤代烃发生消去反应时,被破坏的键是①和③ |
| D、当卤代烃发生消去反应时,被破坏的键是①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④ | B、①②④⑤ | C、③④ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn→Zn2++2e- |
| B、Br2+2e-→2Br- |
| C、2Br-→Br2+2e- |
| D、Zn2++2e-→Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①③⑥ |
| B、只有②④⑥ |
| C、只有①②③④⑥ |
| D、①②③④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com