

分析 (1)A在常温下与水反应生成非金属氧化物E,因此符合条件的是NO2溶于水;
①B是硝酸,当X是碱性溶液,C分子中有22个电子,这说明C是CO2,因此X是碳酸盐;
②B是硝酸,X为金属单质,且X能与C继续反应,说明X应该是变价金属,所以X是铁,C为硝酸铁;
(2)若E为常见单质气体,D为白色胶状沉淀,则D是氢氧化铝,由于氢氧化铝是两性氢氧化物,则符合条件的是B是碱,X是铝盐,C是偏铝酸盐,所以A是钠或过氧化钠,与水反应生成氢氧化钠和氢气或氢氧化钠与氧气;
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应生成C和一种可燃性气体单质,则可推知A为Na2O2,B为O2,氧气与碳反应生成二氧化碳,二氧化碳与碳反应生成 一氧化碳,一氧化碳与水反应生成二氧化碳和氢气,氢气可燃,所以X为C,C为CO2,D为CO,则E为Na2CO3,根据反应CO(g)+H2O(g)?CO2(g)+H2(g)中,K=$\frac{c(C{O}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}$,利用三段式可计算出D的转化率.
解答 解:(1)A在常温下与水反应生成非金属氧化物E,因此符合条件的是NO2溶于水,反应的化学方程式为:3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
①B是硝酸,当X是碱性溶液,C分子中有22个电子,这说明C是CO2,因此X是碳酸盐,CO32-水解溶液显碱性,所以表示X溶液呈碱性的离子方程式为:CO32-+H2O?HCO3-+OH-,CO2是由碳氧双键构成的共价化合物,所以CO2的结构式为O=C=O,故答案为:CO32-+H2O?HCO3-+OH-;O=C=O;
②B是硝酸,X为金属单质,且X能与C继续反应.这说明X应该是变价金属,所以X是铁.则X与B的稀溶液反应生成C的离子反应方程式为Fe+4H++NO3-=Fe3++NO↑+2H2O,故答案为:Fe+4H++NO3-=Fe3++NO↑+2H2O;
(2)若E为常见单质气体,D为白色胶状沉淀,则D是氢氧化铝.由于氢氧化铝是两性氢氧化物,则符合条件的是B是碱,X是铝盐,C是偏铝酸盐.所以A是钠或过氧化钠,与水反应生成氢氧化钠和氢气或氢氧化钠与氧气,因此A的化学式可能是Na 或Na2O2,B为氢氧化钠,氢氧化钠中含有的化学键类型为离子键和极性键,C与X反应的离子方程式为:Al3++3AlO2-+6H2O=4Al(OH)3↓,
故答案为:Na或Na2O2;离子键和极性共价键;Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应生成C和一种可燃性气体单质,则可推知A为Na2O2,B为O2,氧气与碳反应生成二氧化碳,二氧化碳与碳反应生成 一氧化碳,一氧化碳与水反应生成二氧化碳和氢气,氢气可燃,所以X为C,C为CO2,D为CO,则E为Na2CO3,可逆反应的化学方程式为CO(g)+H2O(g)?CO2(g)+H2(g),设起始物质的浓度为a mol/L,转化的CO的浓度为xmol/L,
根据反应CO(g)+H2O(g)?CO2(g)+H2(g),
起始(mol/L) a a 0 0
转化(mol/L) x x x x
平衡(mol/L)a-x a-x x x
K=$\frac{c(C{O}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}$=$\frac{{x}^{2}}{(a-x)^{2}}$=1,所以x=$\frac{1}{2}$a,则CO的转化率为$\frac{\frac{1}{2}a}{a}$×100%=50%,
故答案为:CO(g)+H2O(g)?CO2(g)+H2(g);50%.
点评 本题考查无机物的推断,涉及钠元素单质化合物性质,物质的焰色反应为推断突破口,旨在考查学生对基础知识的掌握,需要学生熟练掌握元素化合物知识,难度中等.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案科目:高中化学 来源: 题型:选择题
| A. | NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O═Fe(OH)2↓+2HC1O | |
| B. | NH4HSO3溶液与足量NaOH溶液反应:NH4++OH-═NH3↑+H2O | |
| C. | NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 将1 mol•L-1NaAlO2溶液和1.5 mol•L-1的HC1溶液等体积混合:6AlO2-+9H++3H2O═5Al(OH)3↓+Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用带橡皮塞的棕色试剂瓶存放浓硝酸 | |
| B. | 容量瓶、分液漏斗使用前均需检查是否漏水 | |
| C. | 分液漏斗分液时,必须先将下层液体从下口放出,再将上层液体从上口倒出 | |
| D. | 蒸馏时,需将温度计的水银球没入液面以下且不接触烧瓶壁 | |
| E. | 氨气喷泉实验时,收集气体的烧瓶必须干燥 | |
| F. | 用玻璃棒蘸取待测液,点在润湿的pH试纸上测定其pH |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 步骤Ⅰ | 称取样品Wg配成溶液置于锥形瓶中,并调节PH≤2.0 |
| 步骤Ⅱ | 向锥形瓶中加入足量KI晶体,充分搅拌,并加入少量指示剂 |
| 步骤Ⅲ | 用c mol/L的Na2S2O3溶液滴定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| B. | 2.24 L CO2中含有的原子数为0.3×6.02×1023 | |
| C. | 200 mL 5 mol•L-1 Na2CO3溶液中,含6.02×1023个CO32- | |
| D. | 4.5gSiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
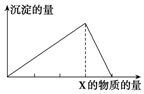 将物质X逐渐加入(或通入)Y溶液中,生成沉淀的量与加入X的物质的量关系如图所示,符合图示情况的是( )
将物质X逐渐加入(或通入)Y溶液中,生成沉淀的量与加入X的物质的量关系如图所示,符合图示情况的是( )| A | B | C | D | |
| X | CO2 | HCl | NaOH | AlCl3 |
| Y | Ca(OH)2 | AlO2- | AlCl3 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
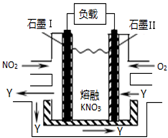 (1)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图.该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为NO2+NO3--e-═N2O5.若生成1molY,则需要消耗标准状况下氧气的体积为5.6L.
(1)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图.该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为NO2+NO3--e-═N2O5.若生成1molY,则需要消耗标准状况下氧气的体积为5.6L.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| B. | 标准状况下,22.4L盐酸含有NA个HC1分子 | |
| C. | 1Lmol•L-1的NaC1O溶液中含有C1O-的数目为NA | |
| D. | 1molNa被完成氧化生成Na2O2,失去个2NA电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com