
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶
液中各种离子的物质的量变化如图所示。有关说法不正确的是( )
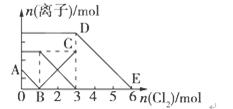
A.线段BC代表Fe3+物质的量的变化情况
B.原混合溶液中n(FeBr2)=3mol
C.当通入2molCl2时,溶液中已发生的离子反应为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.原溶液中n(Fe2+):n(I-):n(Br-)=3∶1∶2
【知识点】本题考查离子方程式的有关计算
【答案解析】D 解析还原性为I->Fe2+>Br-,则先发生2I-+Cl2═I2+2Cl-,I-反应完毕再发生2Fe2++Cl2═2Fe3++2Cl-,最后发生反应2Br-+Cl2═Br2+2Cl-,A.B点时溶液中I-完全反应,溶液中存在Fe2+和Br-,BC段发生2Fe2++Cl2═2Fe3++2Cl-,代表Fe3+的物质的量的变化情况,故A正确;B.由图可知,BC段发生2Fe2++Cl2═2Fe3++2Cl-,Fe2+反应完毕消耗氯气2mol,由方程式可知n(Fe2+)=2×2mol=4mol,由图可知AB段消耗氯气1mol,发生2I-+Cl2═I2+2Cl-,故n(I-)=2n(Cl2)=2mol即n(FeI2)=1mol,则n(FeBr2)=3mol,故B正确;C.AB段发生2I-+Cl2═I2+2Cl-,2mol的I-消耗1mol氯气,BC段发生2Fe2++Cl2═2Fe3++2Cl-,余下的1mol氯气再与2molFe2+反应,故参加反应的n(Fe2+):n(I-)=1:1,故通入2molCl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl-,故C正确;D.由图可知AB段消耗氯气1mol,发生2I-+Cl2═I2+2Cl-,故n(I-)=2n(Cl2)=2mol,BC段发生2Fe2++Cl2═2Fe3++2Cl-,消耗氯气2mol,故n(Fe2+)=2n(Cl2)=2×2mol=4mol,DE段发生2Br-+Cl2═Br2+2Cl-,消耗氯气3mol,故n(Br-)=2n(Cl2)=6mol,故原溶液中n(Fe2+):n(I-):n(Br-)=4mol:2mol:6mol=2:1:3,故D错误;


科目:高中化学 来源: 题型:
从海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。
海水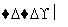

试回答下列问题:
(1)写出用海滩上的贝壳制备Ca(OH)2的化学方程式:_________________________
________________________________________________________________________。
(2)写出电解饱和NaCl溶液的化学方程式:__________________________________。
(3)将电解生成的氯气通入石灰乳可制得漂白粉,其反应的化学方程式为:_______
________________________________________________________________________。
(4)用海滩上的贝壳制Ca(OH)2而不从异地山中开凿石灰石制取,主要考虑到什么问题?
________________________________________________________________________。
(5)从经济效益角度看,该化工厂的厂址应选择在
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
天然橡胶分解后的产物是碳氢化合物,它含C:88.2%,H:11.8%,此气体的相对分子质量是68,求它的化学式。此物质0.5mol能和160gBr2起加成反应,在生成物中溴原子分布在不同的碳原子上,又知溴代物的结构上有一个碳原子是在支链上,根据上述条件写出产物的分子式及结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有等物质的量的铜和银的混合物17.2 g,与50.0 mL
的浓硝酸恰好完全反应,
产生气体4.48 L(标准状况),则下列说法正确的是
A.产生的气体是0.2 mol NO2
B.硝酸的物质的量浓度为12 mol·L-1
C.反应中被还原和未被还原的硝酸物质的量之比为3∶2
D.要使产生的气体恰好完全被水吸收需要通入氧气0.075 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
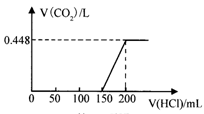
将露置于空气中的某氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的CO2体积(标准状况)与加入的盐酸体积有如图关系(不考虑CO2在水中的溶解)。试计算:(无需书写计算步骤)
(1)盐酸的物质的量浓度为 mol/L。
(2)该样品中NaOH与Na2CO3物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
无色透明的酸性溶液中,能大量共存的是
A.Na+、K+、CO32-、NO3- B.K+、Fe2+、NH4+、NO3-
C.NH4+、Al3+、SO42-、NO3- D.K+、Na+、NO3-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
根据表中信息判断,下列选项不正确的是
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO | Cl2、Mn2+… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO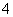 >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断不正确的是
A.与NaOH反应的氯气一定为0.15 mol
B.n(Na+)∶n(Cl-) 可能为7∶3
C.若反应中转移的电子为n mol,则n一定大于0.15 mol
D.n(NaCl)∶n(NaClO)∶n(NaClO3)可能为7∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于能量转化的认识不正确的是( )
A.绿色植物的光合作用是将光能转变为化学能
B.煤燃烧时化学能转变成热能和光能
C.原电池工作时,化学能转变为电能
D.白炽灯工作时,电能全部转变成光能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com