
| 应称取NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它玻璃仪器 |
分析 (1)根据m=CVM来计算需要溶质的质量;依据配制溶液体积及常用容量瓶规格选择合适容量瓶;依据配制一定物质的量浓度溶液一般步骤选择需要仪器;
(2)依据容量瓶构造解答;
(3)根据配制步骤是计算、称量、溶解、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(4)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
解答 解:(1)实验室用NaOH固体配制250mL 1mol/L的NaOH溶液,需要固体氢氧化钠质量m=0.25L×1mol/L×40g/mol=10.0g;
配制250mL 1mol/L的NaOH溶液,需要用到250mL容量瓶;
操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以除容量瓶外还需要的其它玻璃仪器:烧杯、玻璃棒、胶头滴管、量筒;
故答案为:10.0或10 250 玻璃棒、烧杯、胶头滴管、量筒(没答量筒给分);
(2)容量瓶为精密仪器,上面标有温度、容量和刻度线;
故选:①③⑤;
(3)配制步骤是计算、称量、溶解、洗涤、定容、摇匀、装瓶,所以操作顺序是B→C→A→F→E→D,
故答案为:B→C→A→F→E→D;
(4)A、称量NaOH时,因为没有用到游码,所以对称量结果无影响,溶液浓度准确,故A不选;
B、向容量瓶中转移溶液时(实验步骤②)不慎有液滴洒在容量瓶外面,导致溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故B选;
C、加蒸馏水时不慎超过了刻度线,导致溶液体积偏大,溶液浓度偏低,故C选;
D、定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故D不选;
E、配制前,容量瓶中有少量蒸馏水,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故E不选;
故选:BC.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,熟悉配制原理和操作步骤是解题关键,注意依据c=$\frac{n}{V}$进行误差分析的方法,题目难度不大.


科目:高中化学 来源: 题型:推断题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
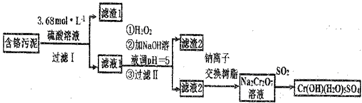
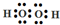 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中溶液变浑浊,一定是CO32- | |
| B. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| C. | 向AlCl3溶液中加入氨水产生白色沉淀,继续滴加至过量沉淀溶解 | |
| D. | 加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 过滤时,引流的玻璃棒下端触在三层滤纸处 | |
| C. | 蒸馏中,冷却水应从冷凝管的下口通入,上口流出 | |
| D. | 用pH试纸测溶液的酸性时,应先将试纸用蒸馏水润湿 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 | |
| B. | 可用25mL碱式滴定管量取20.00 mLKMnO4溶液 | |
| C. | 用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出 | |
| D. | 向乙酸乙酯中加入饱和Na2CO3溶液,振荡,分液除去乙酸乙酯中的少量乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
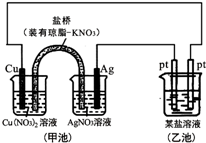
| A. | 图中甲池为原电池装置,电子从铜电极通过溶液和盐桥流向Ag电极 | |
| B. | 实验过程中,甲池左侧烧杯中NO3-的浓度不变 | |
| C. | 若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量不变 | |
| D. | 若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液不可能是AgNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com