

 )外,含有的官能团名称是碳碳双键、酯基;
)外,含有的官能团名称是碳碳双键、酯基; .
. 分析 A→B是两分子乙炔发生加成反应,对比B、C的结构可知,B与甲醇发生加成反应生成C,则M为CH3OH;由F的结构,逆推可知E为CH3C≡CCOOH,则D与二氧化碳发生加成反应生成E,C由F发生加成反应生成G.
(2)根据H的结构判断含有的官能团;
(3)实验室用碳化钙与水反应制备乙炔;
(4)CH3C≡CCOOH与乙醇发生酯化反应生成F;
(5)a.F含有酯基,不属于烃类物质;
b.聚乙烯的单体是氯乙烯;
c.根据H原子守恒计算水的物质的量;
d.H中含有羰基、碳碳双键和酯基,具有酮、烯烃和酯的性质;
(6)TMOB结构中含有苯环,存在甲氧基(CH3O-),又因为除苯环吸收峰外仅有1个吸收峰,所以应该含有3个甲氧基(CH3O-),且三个甲氧基等价.
解答 解:A→B是两分子乙炔发生加成反应,对比B、C的结构可知,B与甲醇发生加成反应生成C,则M为CH3OH;由F的结构,逆推可知E为CH3C≡CCOOH,则D与二氧化碳发生加成反应生成E,C由F发生加成反应生成G.
(1)对比A与B结构可知,A→B是两分子乙炔发生加成反应,对比B、C的结构可知,B与甲醇发生加成反应生成C,则M为CH3OH,
故答案为:加成反应;CH3OH;
(2)根据H的结构可知,H中除了羰基外,含有的官能团名称是:碳碳双键、酯基,
故答案为:碳碳双键、酯基;
(3)实验室用碳化钙与水反应制备乙炔,反应方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑,
故答案为:CaC2+2H2O═Ca(OH)2+C2H2↑;
(4)CH3C≡CCOOH与乙醇发生酯化反应生成F,反应方程式为:CH3C≡CCOOH+HOCH2CH3$→_{△}^{浓硫酸}$CH3C≡CCOOCH2CH3+H2O,
故答案为:CH3C≡CCOOH+HOCH2CH3$→_{△}^{浓硫酸}$CH3C≡CCOOCH2CH3+H2O;
(5)a.F中含有酯基,不属于烃类物质,故a错误;
b.聚乙烯的单体是氯乙烯,A能和HCl发生加成反应生成氯乙烯,所以A和HCl能得到聚氯乙烯的单体,故b正确;
c.G的分子式为C11H16O3,根据H原子守恒知,1mol G完全燃烧生成8molH2O,故c错误;
d.H中含有羰基、碳碳双键和酯基,具有酮、烯烃和酯的性质,所以能发生加成、取代反应,故d正确;
故选:bd;
(6)TMOB结构中含有苯环,存在甲氧基(CH3O-),又因为除苯环吸收峰外仅有1个吸收峰,所以应该含有3个甲氧基(CH3O-),且三个甲氧基等价,则TMOB的结构简式为: ,
,
故答案为: .
.
点评 本题考查有机物推断、有机物结构与性质等,根据已知物质结构、反应条件进行推断,注意根据结构简式理解化学键的断裂与形成,侧重考查分析推断能力,难度中等.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 在标准状态下,1L庚烷完全燃烧后,所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 1mol碳正离子CH5+所含的电子数为11NA | |
| C. | 标准状态下,16g甲烷完全燃烧所消耗的氧气的分子数为2NA | |
| D. | 0.5molC3H8分子中含C-H共价键2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH2-CH2-CH2-CH3和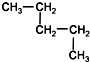 | B. | 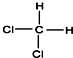 和 和 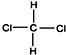 | ||
| C. | CH3-CH3和CH3-CH2-CH3 | D. | 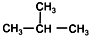 和CH3-CH2-CH2-CH3 和CH3-CH2-CH2-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
 ,丁的结构式
,丁的结构式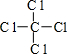
 ,最高价氧化物的水化物化学式为HClO4.
,最高价氧化物的水化物化学式为HClO4.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
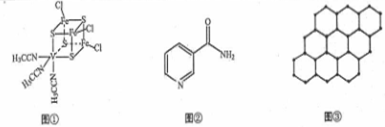
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
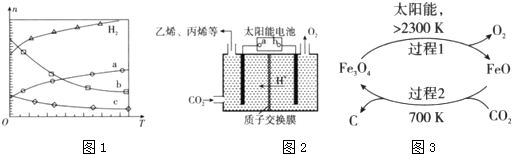
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:乙烷>戊烷>2-甲基丁烷 | B. | 熔点:Al>Na>Na和K的合金 | ||
| C. | 密度:苯<水<1,1,2,2-四溴乙烷 | D. | 热稳定性:HF>HCl>H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属铯的熔点比金属钠高 | B. | CsOH比NaOH的碱性强 | ||
| C. | Cs与H2O能剧烈反应,但没有钠剧烈 | D. | 碳酸铯难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com