
(14分)
以锌锰废电池中的碳包(含碳粉、Fe、Cu、Ag和MnO2等物质 )为原料回收MnO2的工艺流程如下:
I. 将碳包中物质烘干,用足量稀HNO3溶解金属单质,过滤,得滤渣a;
II. 将滤渣a在空气中灼烧除去碳粉,得到粗MnO2;
III. 向粗MnO2中加入酸性H2O2溶液,MnO2溶解生成Mn2+,有气体生成;
IV. 向III所得溶液(pH约为6)中缓慢滴加0.50 mol?L-1 Na2CO3溶液,过滤,得滤渣b,其主要成分为MnCO3;
V. 滤渣b经洗涤、干燥、灼烧,制得较纯的MnO2。
(1)Ι中Ag与足量稀HNO3反应生成NO的化学方程式为 。
(2)已知II的灼烧过程中同时发生反应:
MnO2(s) + C(s) === MnO(s) + CO (g) △H = +24.4 kJ ? mol – 1 ①
MnO2(s) + CO(g) === MnO(s) + CO2(g) △H = -148.1 kJ ? mol – 1 ②
写出MnO2和C反应生成MnO和CO2的热化学方程式: 。
(3)H2O2分子中含有的化学键类型为 、 。
(4)III中MnO2溶解的离子方程式为 ,溶解一定量的MnO2,H2O2的实际消耗量比理论值高,用化学方程式解释原因: 。
(5)IV中,若改为“向0.50 mol?L-1 Na2CO3溶液中缓慢滴加III所得溶液”,滤渣b中会混有较多Mn(OH)2沉淀,解释其原因: 。
(6)V中MnCO3在空气中灼烧的化学方程式为 。
(14分)
(1)3Ag + 4HNO3 === 3AgNO3 +NO? + 2H2O
注:写“△”不扣分,写成离子方程式不扣分。
(2)2MnO2(s) + C(s) === 2MnO(s) + CO2(g) △H = -123.7 kJ ? mol -1
 (3)极性键、非极性键 注:每空各1分,只写“共价键”的扣1分。
(3)极性键、非极性键 注:每空各1分,只写“共价键”的扣1分。
(4)MnO2 + H2O2 + 2H+ === Mn2+ + O2? + 2H2O; 2H2O2 ==== O2?+ 2H2O
 (5)Na2CO3溶液pH>7显碱性,III所得溶液pH约为6 显弱酸性(1分),后者滴加到前者中,溶液中c(OH-)较大,Mn2+与OH-生成Mn (OH)2沉淀(或答CO32-的水解平衡正向移动生成Mn (OH)2沉淀)(1分)。
(5)Na2CO3溶液pH>7显碱性,III所得溶液pH约为6 显弱酸性(1分),后者滴加到前者中,溶液中c(OH-)较大,Mn2+与OH-生成Mn (OH)2沉淀(或答CO32-的水解平衡正向移动生成Mn (OH)2沉淀)(1分)。
(6)2MnCO3 + O2 === 2MnO2 + 2CO2 注:写“加热”、“高温”不扣分。
【解析】
试题分析:(1)Ag与足量稀HNO3反应生成NO的化学方程式为3Ag + 4HNO3 === 3AgNO3 +NO? + 2H2O
(2)根据盖斯定律目标方程式= ① +②,所以MnO2和C反应生成MnO和CO2的热化学方程式为2MnO2(s) + C(s) === 2MnO(s) + CO2(g) △H = -123.7 kJ ? mol -1
(3)过氧化氢是共价化合物,分子中含有极性共价键、非极性共价键;
(4)MnO2中加入酸性H2O2溶液,MnO2溶解生成Mn2+,有气体生成;锰元素的化合价降低,则过氧化氢中氧元素的化合价升高,所以该气体是氧气,离子方程式为MnO2 + H2O2 + 2H+ === Mn2+ + O2? + 2H2O;因为过氧化氢在二氧化锰存在的条件下会发生分解反应,生成氧气和水,用化学方程式表示为
 2H2O2 ==== O2?+ 2H2O;
2H2O2 ==== O2?+ 2H2O;
(5)Na2CO3溶液水解使溶液pH>7显碱性,III所得溶液pH约为6 显弱酸性(1分),后者滴加到前者中,氢离子与水解生成的碳酸氢根离子反应生成二氧化碳气体,使水解平衡正向移动,溶液中c(OH-)较大,Mn2+与OH-生成Mn (OH)2沉淀;
 (6)MnCO3在空气中灼烧的反应类似与碳酸钙的分解反应,化学方程式为
(6)MnCO3在空气中灼烧的反应类似与碳酸钙的分解反应,化学方程式为
2MnCO3 + O2 === 2MnO2 + 2CO2
考点:考查对化学方程式的记忆,由所给条件判断反应方程式及书写,化学键类型的判断,盖斯定律得应用,对工业流程的分析


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:2013-2014北京市西城区高三二模理综化学试卷(解析版) 题型:选择题
在2 L的密闭容器中进行如下反应: CO(g)+H2O(g) CO2(g)+H2(g),有如下数据:
CO2(g)+H2(g),有如下数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | |||
CO | H2O | CO2 | H2 | CO2 | ||
1 | 650 | 2.0 | 1.0 | 0 | 0 | 0.8 |
2 | 800 | 2.0 | 2.0 | 0 | 0 | 1.0 |
下列说法正确的是
A.正反应为吸热反应
B.实验1中,CO的转化率为80%
C.650℃时,化学平衡常数K=8/3
D.实验1再加入1.0 mol H2O,重新达到平衡时,n (CO2)为1.6 mol
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市西城区下学期高一年级期末考试化学试卷(解析版) 题型:填空题
(5分)某实验小组同学进行如下实验,以探究化学反应中的能量变化。

(1)实验表明:①中的温度降低,由此判断氢氧化钡晶体与氯化铵晶体反应是____________(填“吸热”或“放热”)反应。
(2)实验②中,该小组同学在烧杯中加入5 mL 1.0 mol/L盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,如图A所示,该反应是____________(填“吸热”或“放热”)反应,其能量变化可用下图中的____________(填“B”或“C”)表示。
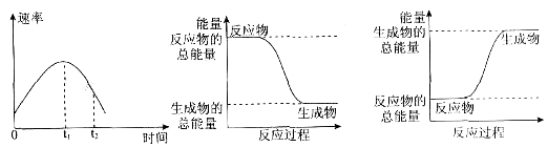
图A中0一tl段化学反应速率变化的原因是_________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市西城区下学期高一年级期末考试化学试卷(解析版) 题型:选择题
下列物质中,在一定条件下既能发生加成反应,也能发生取代反应,但不能使KMnO4酸性溶液褪色的是
A.乙烷B.苯C.乙烯D.乙醇
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市海淀区高三第二学期二模理综化学试卷(解析版) 题型:选择题
下列化学用语不能正确解释相关事实的是
A.碱性氢氧燃料电池的正极反应:H2 - 2e- + 2OH-=== 2H2O
B.用电子式表示NaCl的形成过程: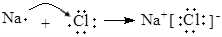
C.向含有Hg2+的废水中加入Na2S可除去Hg2+:Hg2+ + S2- === HgS↓
D.汽车尾气系统的催化转化器可降低NO等的排放:2CO + 2NO 催化剂 2CO2 +N2
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市朝阳区高三二模理综化学试卷(解析版) 题型:简答题
(16分)
高分子化合物PPTA树脂、PF树脂、脲醛树脂合成路线如下。
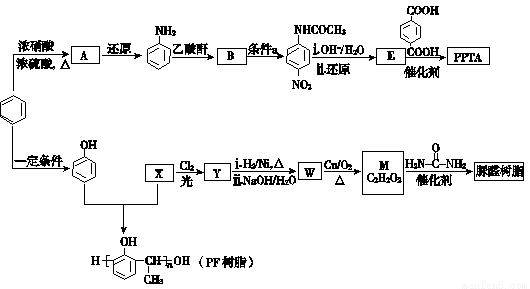
已知:I. R—NH2 +  R—NHCOCH3 + CH3COOH (R为烃基)
R—NHCOCH3 + CH3COOH (R为烃基)
(乙酸酐)
II. 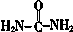 (尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子。
(尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子。
(1) 由苯合成A 的化学方程式是 。
(2)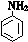 →B的反应类型是 。
→B的反应类型是 。
(3)条件a选择的化学试剂是 。
(4)E中有两种不同化学环境的氢原子,PPTA树脂的结构简式是 。
(5)高分子化合物PF树脂的单体是苯酚和 。
(6)W中只有一种含氧官能团。下列说法正确的是 。
a. Y分子中只有一种官能团
b. M与HCHO互为同系物
c. W的沸点高于C2H6
(7)Y→W时,条件ⅰ、ⅱ转化的官能团分别是 、 。
(8)合成脲醛树脂的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市第二学期期中测试高二化学试卷(解析版) 题型:选择题
将用于2008年北京奥运会的国家游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成全氟乙丙烯。下列说法错误的是
A.ETFE分子中可能存在“-CH2-CH2-CF2-CF2-”的连接方式
B.合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应
C.聚全氟乙丙烯分子的结构简式可能为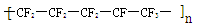
D.四氟乙烯中既含有极性键又含有非极性键
查看答案和解析>>
科目:高中化学 来源:2014年全国普通高等学校招生统一考试理科综合能力化学(福建卷解析版) 题型:选择题
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
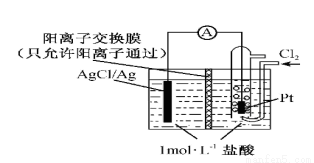
A.正极反应为AgCl +e-=Ag +Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com