
| A | B | C | D | |
| 强电解质 | Fe | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | CO2 | HClO | Fe(OH)3 |
| 非电解质 | 蔗糖 | BaSO4 | 酒精 | H2O |
| 混合物 | 漂白粉 | 胆矾 | 盐酸 | 液氯 |
| A. | A | B. | B | C. | C | D. | D |
分析 强电解质是指在水中完全电离成离子的化合物;弱电解质是指在水中不完全电离,只有部分电离的化合物;在水溶液里和熔融状态下都不导电的化合物是非电解质,单质和混合物既不是电解质也不是非电解质,混合物是不同种物质组成的,据此进行判断.
解答 解:A、金属铁属于单质,不属于电解质,故A错误;
B、二氧化碳属于非电解质,硫酸钡是强电解质,胆矾属于纯净物,故B错误;
C、碳酸钙属于强电解质,次氯酸是弱酸,属于电解质,酒精是非电解质,盐酸属于混合物,故C正确;
D、水属于弱电解质,液氯属于纯净物,故D错误.
故选C.
点评 本题考查了强电解质、弱电解质和非电解质的判断,难度不大,明确电解质的强弱与电离程度有关,不能根据电解质溶液的导电性强弱划分强弱电解质.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | lNA | B. | 2NA | C. | 3NA | D. | 0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 编号 | 实验 | 现象 |
| ① | 放入蒸馏水 | 木条燃烧 |
| ② | 放入Na2SiO3饱和溶液 | 木条不燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验方案 | 实验现象 |
| 1.用砂纸擦后的镁带与沸水反应,再向反应液中滴加酚酞 2.向新制的H2S饱和溶液中滴加新制的氯水 3.钠与滴有酚酞试液的冷水反应 4.镁带与2mol/L的盐酸反应 5.铝条与2mol/L的盐酸反应 6.向AlCl3溶液中滴加NaOH溶液至过量 | A.浮于水面,熔成小球,四处游动,逐渐缩小,溶液变红色 B.产生大量气体,气体可燃,溶液变浅红色 C.反应不十分强烈,产生的气体可燃 D.剧烈反应,产生的气体可燃 E.生成白色絮状沉淀,继而沉淀消失 F.生成淡黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 方便添加木柴 | B. | 升高木柴的温度 | ||
| C. | 降低木柴的着火点 | D. | 使木柴与空气充分接触 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
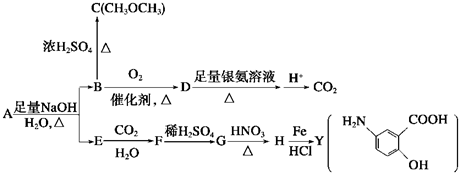
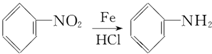
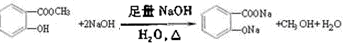 .
.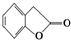 和
和 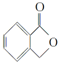 ,鉴别I和J的试剂为FeCl3或浓溴水.
,鉴别I和J的试剂为FeCl3或浓溴水.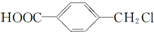 制得,写出K在浓硫酸作用下生成的聚合物的结构简式:
制得,写出K在浓硫酸作用下生成的聚合物的结构简式: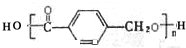 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com