
����Ŀ����ԭ�����ǻ���������ʵ�����г��õĻ�ԭ������ҵ�����̷�Ϊԭ���Ʊ���ԭ���۵Ĺ������£�
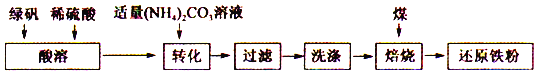
�ش��������⣺
��1�����ܹ����������������________________________ ��
��2��ת����Ŀ�����Ƶ�FeCO3����ҺʱӦ��(NH4)2CO3��Һ���뵽FeSO4�У�ԭ����_____________��
��3��ת���������¶Ȳ�����35�棬ԭ����___________________________ ��
��4�����ɵ�FeCO3��������ϴ�ӣ�����ϴ���Ƿ���ȫ�ķ�����___________________ ��
��5����FeCO3��Һ��¶�ڿ����У���������Ϊ���ɫ��ͬʱ�ͷų�CO2��д���÷�Ӧ�Ļ�ѧ����ʽ��________________________ ��
��6���ڱ��չ����������CaCO3��������������ͼΪ��CaCO3�Ͳ���CaCO3�Ի�ԭ���۲��ʵ�Ӱ�죬��ͼ����CaCO3����һ����Ϊ________________________ ��

���𰸡� ����Fe2+ˮ�� ��ֹ�������������� ��ֹ(NH4)2CO3���ȷֽ� ȡ���һ��ϴ����Һ1~2mL���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ� 4FeCO3+6H2O+O2==4Fe(OH)3+4CO2 �ֽ������CO2��C��Ӧ���ɻ�ԭ��CO
����������1���̷�����ˮ�õ�������������Һ��Fe2+��ˮ�⣬���ܹ��������������������Fe2+ˮ�⣻��2��ת����Ŀ�����Ƶ�FeCO3����ҺʱӦ��(NH4)2CO3��Һ���뵽FeSO4�У���ֹ������������������3��(NH4)2CO3�����ֽ⣬Ϊ�˼���(NH4)2CO3��Һ�ļ��٣�ת��������Ӧ�����¶���35 �����£���ֹ(NH4)2CO3���ȷֽ⣻��4�����ɵ�FeCO3��������ϴ�ӣ�����ϴ���Ƿ���ȫ�ķ�����ȡ���һ��ϴ����Һ1~2mL���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���(5)���ɫ������Fe(OH)3��FeCO3��H2O��O2��Ӧ����Fe(OH)3��CO2����Ӧ�Ļ�ѧ����ʽΪ��4FeCO3+6H2O+O2==4Fe(OH)3+4CO2����6�������£�̼��Ʒֽ����ɶ�����̼��������̼�ܱ�̼��ԭ����һ����̼�����Լ���̼���������һ����̼�ĺ�������ԭ���۵IJ�������


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�����������������Ӧ�ù㷺��
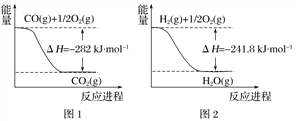
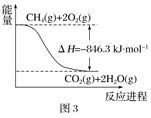
(1)�ϳɰ��õ�H2����CH4Ϊԭ���Ƶ����йػ�ѧ��Ӧ�������仯����ͼ��ʾ����CH4(g) ��H2O(g)��Ӧ����CO(g)��H2(g)���Ȼ�ѧ����ʽΪ________________________________________________��
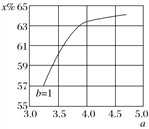
(2)������ȡ����[CO(NH2)2]�ĺϳ����з�����Ӧ��2NH3(g)��CO2(g)![]() CO(NH2)2(l)��H2O(g)����ͼΪ�ϳ����в�ͬ��̼��a[n(NH3)/n(CO2)]��ˮ̼��b[n(H2O)/n(CO2)]��1ʱ������̼ת����(x%)������ͼ���뻭������ͬ��������a��3.5��4.5��Χ����b[n(H2O)/n(CO2)]��1.5ʱ�Ķ�����̼ת����(x%)������ͼ��_______��
CO(NH2)2(l)��H2O(g)����ͼΪ�ϳ����в�ͬ��̼��a[n(NH3)/n(CO2)]��ˮ̼��b[n(H2O)/n(CO2)]��1ʱ������̼ת����(x%)������ͼ���뻭������ͬ��������a��3.5��4.5��Χ����b[n(H2O)/n(CO2)]��1.5ʱ�Ķ�����̼ת����(x%)������ͼ��_______��
(3)��������(NaN3)������������ȫ����������ҵ����NaN3��Ҫ����175 ��ʱ��NaNO3��ĩ�ӵ��ۻ���NaNH2��������������ֳ����ļ�����������д���������̵Ļ�ѧ����ʽ��__________________��
(4)������(HN3)��һ��һԪ��������ˮ��Һ�д�����HN3![]() H����N
H����N![]() �������½�a mol NaN3���뵽b L c mol��L��1��HN3��Һ����������Һ��������������¶���HN3�ĵ���ƽ�ⳣ��Ka��____________(�ú���ĸ�Ĵ���ʽ��ʾ��������Һ����仯)��
�������½�a mol NaN3���뵽b L c mol��L��1��HN3��Һ����������Һ��������������¶���HN3�ĵ���ƽ�ⳣ��Ka��____________(�ú���ĸ�Ĵ���ʽ��ʾ��������Һ����仯)��
(5)�ǰ�NH2OH���Կ�����NH3�����ڵ�һ����ԭ�ӱ��ǻ�ȡ������������������������ˮ��Һ������ʽ��е�����ڹ��缫��NO![]() ��ת��ΪNH2OH���Բ�Ϊ��һ������õ�ⷴӦ���ܻ�ѧ����ʽΪ_____________________________________________________________��
��ת��ΪNH2OH���Բ�Ϊ��һ������õ�ⷴӦ���ܻ�ѧ����ʽΪ_____________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ����ͭ��CuO+H2=Cu+H2O���ڸ÷�Ӧ�У�������
A.CuO����ԭ��
B.CuO��������
C.ͭԪ�ػ��ϼ۽���
D.ͭԪ�ػ��ϼ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����鶯�����֭�к����Ϸḻ�����Ǿ������������γ� �� ��
A��������+���� B��������+������
C��������+������ D������+������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯��Ҫ��������������ʵ�ֵ���
A.H2O2��O2 B.HCl��Cl2C.H2SO4 ��BaSO4D.CuO��Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����6molA�����5molB�����Ϸ���4L�ܱ������У���һ�������·�����Ӧ��3A ��g��+B��g��2C��g��+xD��g������5min�ﵽƽ�⣬��ʱ����CΪ2mol���ⶨD��ƽ����Ӧ����Ϊ0.1mol/��Lmin��������˵��������ǣ�������
A.x=2
B.B��ת����Ϊ20%
C.ƽ��ʱA��Ũ��Ϊ0.75mol/L
D.���´�ƽ��ʱ�����ڵ�ѹǿΪ��ʼʱ��85%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ����������ϵ���
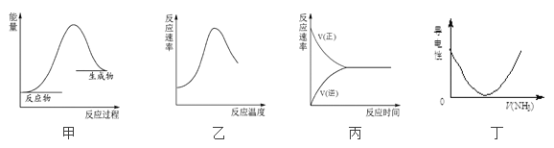
A. ͼ�ױ�ʾȼ��ȼ�շ�Ӧ�������仯
B. ͼ�ұ�ʾø����Ӧ�ķ�Ӧ�����淴Ӧ�¶ȵı仯
C. ͼ����ʾ���淴Ӧ�Ӽ��뷴Ӧ�↑ʼ������ѧƽ��Ĺ���
D. ͼ����ʾ��NH3ͨ�������Һ�Ĺ����У���Һ�����Եı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�͵��ǵ����Ϻ����ḻ������Ԫ�ء���������Ļ�ѧ����ѧ������ѧ�о����������������û�ʯȼ�ϣ�����������Ի����ĸ���Ӱ�졣
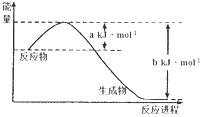
��1����ͼ��25����101kPaʱ��1molNO2�����1molCO��Ӧ����CO2��NO�����������仯ʾ��ͼ��д���÷�Ӧ���Ȼ�ѧ����ʽ____________________________________��
��2���ڲ�ͬ�¶��£���2L�ܱ������м���1molNO��1mol����̿��������Ӧ��2NO(g)+C(s)![]() N2(g)+CO2(g),�ﵽƽ��ʱ���������£�
N2(g)+CO2(g),�ﵽƽ��ʱ���������£�
�¶� | n(C)/mol | n(CO2)/mol |
T1 | 0.3 | |
T2 | 0.6 |
��ش��������⣺
��T1��ʱ���÷�Ӧ��ƽ�ⳣ��K=___________��
��T2��ʱ���������жϸ÷�Ӧ�ﵽƽ��״̬����___________(�����)��
A��v(CO2)��=2v(NO)�� B����������ƽ����Է����������ٱ仯
C�����������ܶȲ��ٱ仯 D��N2��CO2�����ʵ���֮�Ȳ��ٱ仯
��T2��ʱ������ƽ����ٳ���0.4molNO��0.3molCO2��ƽ����___________(��������������������������)�ƶ���
������H<O,��T1___________T2(����>������<��)��
��3����ⷨ��������������������ɻ������ᡣʵ����ģ���ⷨ����NOx��װ������ͼ��ʾ��
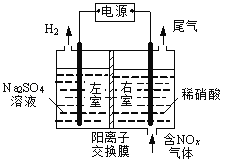
������NO2�������ģ���ⷨ����ʵ�飬д��NO2������Ӧ�ĵ缫��Ӧʽ________________��
�����б����2.24LNO�����գ�ͨ�������ӽ���Ĥ��H+Ϊ___________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������п��صĵ缫��ӦΪпƬ��Zn+2OH--2e-=ZnO+H2O��̼����O2+2H2O+4e-=4OH-���ݴ��жϣ�пƬ�ǣ� ��
A.����������ԭB.������������
C.����������ԭD.������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com