
下列各组混合物无论以何种比例混合,只要总的物质的量一定,完全燃烧时消耗氧气的量是定值的是( )
A.CH2O、C2H4O2、C6H12O6
B.C6H6 、C5H12 、C7H6O2
C.CH2=CH2 、C2H5OH、HOCH2CH2COOH
D.H2 、CO CH3OH
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品。苹果酸(  )是这种饮料的主要酸性物质。下列相关说法不正确的是( )
)是这种饮料的主要酸性物质。下列相关说法不正确的是( )
A.苹果酸在一定条件下能发生酯化反应
B.苹果酸在一定条件下能发生催化氧化反应
C.苹果酸在一定条件下能发生消去反应
D.1 mol苹果酸与Na2CO3溶液反应,必需消耗2 mol Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,有一种叫Thibacillus Ferroxidans的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:
4CuFeS2+2H2SO4+17O2===4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中Fe的化合价为+2,上述反应中被氧化的元素是________。
(2)工业生产中利用上述反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):
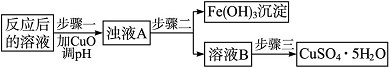
①分析下列表格(其中Ksp是相应金属氢氧化物的沉淀溶解平衡常数):
| Ksp | 氢氧化物开始 沉淀时的pH | 氢氧化物沉淀 完全时的pH | |
| Fe3+ | 2.6×10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
步骤一应调节溶液的pH范围是__________,请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因________________________________________________
________________________________________________________________________。
②步骤三中的具体操作方法是_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式如右图,
则此有机物可发生的反应类型有:
①取代 ②加成 ③消去 ④酯化 ⑤水解⑥氧化 ⑦中和( )
A.①②③⑤⑥ B.②③④⑤⑥ C.①②③④⑤⑥ D.①②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A与乙酸无论以何种比例混合,只要质量一定,完全燃烧后产生的水的质量也一定,试回答:
⑴若A与乙酸相对分子质量相等,且既能发生银镜反应又能发生酯化反应,则A的结构简式为_____________。
⑵若A的相对分子质量为乙酸的1.5倍, 1mol A分别跟足量NaHCO3和足量钠反应可生成1mol CO2和1mol H2,且2molA在浓硫酸存在下可生成1mol含六元环的化合物B,则A的结构简式为 ,写出由A生成B的化学方程式
⑶若A分子中C、H元素质量分数之和为86.67%,其余为O,且A的相对分子质量小于200,则A的分子式为___________。如果A分子中每个碳原子都以单键相结合,且能与金属钠反应产生氢气,则A的结构简式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
100 mL 2 mol/L H2SO4 与过量Zn粉反应,在一定温度下,为了加快反应速率,但又不影响生成氢气的总量,可以采取的措施是( )
A.加入碳酸钠固体 B.改用18 mol/L的浓H2SO4
C.滴入少量硫酸铜溶液 D.加入硫酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于甲烷性质叙述中不正确的是 ( )
A.甲烷是一种无色无味的气体 B.甲烷的密度比空气的密度小
C.甲烷极难溶解于水 D.甲烷性质稳定,不和其它物质反应
查看答案和解析>>
科目:高中化学 来源: 题型:
研究NO2、SO2.CO等大气污染气体的处理具有重要意义。
(1) NO2可用水吸收,相应的化学反应方程式为__________ ___ 利用反应6 NO2+8NH3 7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2,在标准状况下是_____________L。
7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2,在标准状况下是_____________L。
(2)已知:2SO2(g)+O2(g)  2SO3(g) △H=-196.6kJ·mol-1
2SO3(g) △H=-196.6kJ·mol-1
2NO(g)+O2(g) 2NO2(g) △H=-113.0 kJ·mol -1
2NO2(g) △H=-113.0 kJ·mol -1
则反应NO2(g) SO2(g)+ NO2的△H=________ kJ·mol -1 一定条件下,将NO2与SO2以体积比之于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________
SO2(g)+ NO2的△H=________ kJ·mol -1 一定条件下,将NO2与SO2以体积比之于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO2和NO的体积比保持不变 D.每消耗1molSO3的同时生成1mol NO2 测得
上述反应平衡是NO2与SO2体积比为1:6则平衡比常数k=________
| |
| |
 CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H___0(填“>”或“<”)实际生产条件控制在250℃、1.3ⅹ104 kPa左右,选择此压强的理由是_______。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H___0(填“>”或“<”)实际生产条件控制在250℃、1.3ⅹ104 kPa左右,选择此压强的理由是_______。 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com